Фенилпропионовая кислота
Cтраница 2
Получают взаимодействием метилового эфира 3 5-ди-грег - бутил-4 - гидроксИ фенилпропионовой кислоты с тиодиэтиленгликолем в присутствии катализатора. [16]
Так, бензойная кислота СцНпСООН и фенилуксусная кислота C6H5CH2COOH не расщепляются, в то время как фенилпропионовая кислота СбНг СН2СН2СООН превращается в бензойную кислоту СбНсСООН, фенилмасляная кислота СбН5СН2СН2СН2СООН - в фенилуксуспую С6Н5СН2СООН, а фенилва-лериановая кислота СбНг СН. [17]
По этой же методике из этилового эфира а-бензилацетоуксус-ной кислоты может быть получена с 85 % - ным выходом а-окси-мшю-р фенилпропионовая кислота. [18]
Фенил-азо) - 1-нафтиламин 61 4 - ( Фенил-азо) - 1-нафтол 61 Фенилдиазоний хлористый 97 Фенилпиридин 117 р - Фенилпропионовая кислота 117 N-Фенялсукцинимид 90 Фенилуксусная кислота 80, 117 Р - Фенилэтиламин 84 Фенол 96, 135, 140, 161, 165, 168 Фенолфталеи - н 165 Фика закон 24 и ел. [19]
На рис. 76 приведена аналогичная зависимость для той же реакции в присутствии 0 002 М фенилуксусной кислоты ( прямая 2) и в присутствии 0 002 М фенилпропионовой кислоты ( прямая 3), являющихся ингибиторами карбоксипептидазы. [21]
Фенилпропанальдоксим 411 2 - Фенилпропанальдоксимацетат 411 1 - Фенил-1 - пропанол 296 1 - Фенил-2 - пропанол 239 2 - Фенил-2 - пропанол 91 З - Фснил-1 - пропанол 229, 441 1 - Фенилпропен 470 1 - Фенил-1 - пропиламии 286 1 - Фенил-1 - пропилтозилат 239 Фенилиропиоловая кислота 409 р - Фснилпрошгонилхлорид 443 2 - Фенилпропионитрил 411 () - 2 - Фенилпропионовая кислота 460 р - Фенилпропионовый альдегид 443 Фенилсульфаминовая кислота 475 N-Фенил - о-толуамид 322 Фенилтрихлорметилкарбинол 290 Фенилтрихлорсилан 260 Фенилуксуспая кислота 474 константа ио. [22]
Изучение механизма изомеризации неустойчивого промежуточного соединения I определенно показало, что во время перемещения группы R от углерода к азоту она никогда не становится совершенно свободной. Тот же самый чистый оптический изомер можно получить из азида ( - j -) 2-метил - З - фенилпропионовой кислоты путем перегруппировки Курциуса [ И ] и из производных ( - -) 2-метил - 3-фенилпропио-нилгидроксамоврй кислоты путем перегруппировки Лоссена. [23]
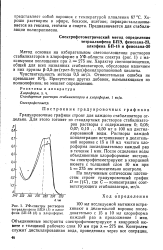 |
УФ-спектры растворов тетраалкофена БПЭ ( и алкофена БП-18 ( 2 в хлороформе. [24] |
Метод основан на избирательном светопоглощении растворов стабилизаторов в хлороформе в УФ-области спектра ( рис. 1) с максимумом поглощения при К - 275 нм. Характер светопоглощения, общий для всех названных стабилизаторов, обусловлен наличием в них группы р - 3 5-ди ( г / 7ег - бутил) фенилпропионовой кислоты. [25]
Лимитирующей стадией процесса является расщепление О-О - связи. При распаде грег-бутиловых перэфиров замещенных уксусных67, пропионовых69 и масляных69 кислот после декарбоксилирования образуются соответствующие радикалы, среди которых наиболее устойчив бензильный радикал из перэфи-ра фенилуксусной кислоты. Однако фенильная группа не оказывает заметного влияния на устойчивость 2-фенилэтильного радикала из перэфира фенилпропионовой кислоты и 3-фенилпропиль-ного радикала из фенилмасляной кислоты. Бутильный радикал из перэфира триметилуксусной кислоты и трихлорметильный радикал из перэфира трихлоруксусной кислоты обладают одинаковой устойчивостью. [26]
Лимитирующей стадией процесса является расщепление О-О - связи. При распаде грег-бутиловых перэфиров замещенных уксусных67, пропионовых69 и масляных 69 кислот после декарбоксилирования образуются соответствующие радикалы, среди которых наиболее устойчив бензильный радикал из перэфи-ра фенилуксусной кислоты. Однако фенильная группа не оказывает заметного влияния на устойчивость 2-фенилэтильного радикала из перэфира фенилпропионовой кислоты и 3-фенилпропиль-ного радикала из фенилмасляной кислоты. Бутильный радикал из перэфира триметилуксусной кислоты и трихлорметильный радикал из перэфира трихлоруксусной кислоты обладают одинаковой устойчивостью. Скорость распада перэфиров замещенных по ядру фенилуксусных кислот68 линейно зависит от константы заместителей аг. [27]
 |
Эфиры ментола. [28] |
Все эти эфиры получались из соответствующих хлорангидридов кислот при взаимодействии последних с ментолом; продукт реакции перегонялся с водяным паром в присутствии 10 % - ного раствора соды и остаток тщательно фракционировался в хорошем вакууме. Эфир бензойной кислоты, полученный и описанный ранее Артом [6], эфир п-толуиловой кислоты и эфир фенилпропионовой кислоты представляют собой твердые вещества. Два первых эфира исследовались в бензольном растворе, последний изучался также и в расплавленном состоянии. Остальные эфиры являются жидкостями, не кристаллизующимися иногда даже при сильном охлаждении. [29]
При применении в качестве катализатора палладия, осажденного на углекислом кальции 18, метод был использован для количественного определения галоида в различных соединениях, например в иодбен-золе, бромбензойной кислоте и в галоидозамещенных жирного ряда. По этому способу из хлоркро-тоновой кислоты образуется кротоновая кислота, между тем как из о-хлоркоричной кислоты получается фенилпропионовая кислота. [30]
Страницы: 1 2 3