Фенолкарбоновая кислота
Cтраница 2
Некоторые фенолкарбоновые кислоты отщепляют при нагревании углекислоту и могут быть затем идентифицированы при помощи обычных для фенолов методов. [16]
Состав фенолкарбоновых кислот был исследован методом хроматографии на бумаге с использованием достоверных образцов некоторых кислот. [17]
Синтез фенолкарбоновых кислот при нагревании фенолятов щелочных металлов с оксидом углерода ( IV) известен под названием реакции Кольбе - Шмитта. [18]
Синтез фенолкарбоновых кислот и флавоноидов резко активируется на свету. Метаболические ингибиторы, подавляющие фотосинтетическую активность хлоропластов ( симазин, диурон, хлорам-феникол), одновременно тормозят и биосинтез флавоноидов. В хло-ропластах зеленых листьев растений локализуются фенольные соединения, некоторые из которых специфичны только для этих орга-нелл. В хлоропластах весенних листьев ивы содержится больший набор фенолов и в большем количестве, чем в хлоропластах осенних листьев. Синтез фенолов в хлоропластах зависит от света. В про-пластидах этиолированных побегов ивы фенолов не содержится. Фенолкарбоновые кислоты и халконы локализуются в клеточном соке. Свет вызывает появление флавонолов в хлоропластах и цитоплазме. [19]
При нагревании фенолкарбоновые кислоты, причем особенно гладко полифенолкарбоновые кислоты, подвергаются декарбоксилированию, превращаясь в соответствующий фенол и двуокись углерода. Подобная лабилизация карбоксила фенолышм гидроксилом происходит только в том случае, если обе группы находятся в орто - или пара-положении друг к другу. [20]
Халкон и фенолкарбоновые кислоты, присутствующие в этиолированных побегах ивы, можно рассматривать как потенциальные предшественники флавоноидов, синтезируемых на свету. [21]
По свойствам Фенолкарбоновая кислота № 1 ( голубое свечение в УФ-свете) была похожа на кофейную или хлорогеновую кислоту, поэтому ее хроматографическое разделение проводили совместно с этими веществами-метчиками. Результаты идентификации этой фе-нолкарбоновой кислоты показали, что она сходна по Rf, по цветным реакциям и по ИК-спектру с кофейной кислотой. [22]
Поэтому из фенолкарбоновых кислот получаются метиловые эфиры метоксилированных кислот. [23]
Кислый характер фенолкарбоновых кислот позволяет обнаружить их бромкрезоловым зеленым ( реактив № 22); разумеется, при применении кислых растворителей кислота должна быть предварительно удалена со слоя. [24]
Кислый характер фенолкарбоновых кислот позволяет обнаружить их бромкре оловым зеленым ( реактив № 22); разумеется, при применении кислых растворителей кислота должна быть предварительно удалена со слоя. [25]
Для синтеза фенолкарбоновых кислот могут быть пригодны любые реакции из числа тех, t помощью которых в бензольное ядро вводится гидроксильная или карбоксильная группа. Этот синтез будет рассмотрен на примере салициловой кислоты. [26]
Синергисты индо - Фенолкарбоновые кислоты: протокаяеховая, ко-лйлуксусной кис - фейная, сиреневая, синаповая, галловая, хлоро-лоты ( ИУК), или геновая. [27]
Антагоняоты ИУК, Фенолкарбоновые кислоты: салициловая, л-окся-илн кофакторы бензойная, ванилиновая, ft - кумаровая. [28]
Другие фенолы и фенолкарбоновые кислоты, например фенол, орсин, / г-оксибензойная кислота, а - и [ 3-резорциловые кислоты, не дают реакции; тимол дает бледно-желтое окрашивание; пирокатехин-оливково-коричневатое; резорцин-оранжевое; гидрохинон-коричневатое; пирогаллол-коричневато-желтое; флороглюцин образует оранжево-желтую муть; хинная кислота дает желтое окрашивание; галловая кислота-оливково-зе-леное; таннин-коричневато-желтое; 3 4-диоксикоричная кислота-оливково-коричневое; протокатеховая и пирогаллолкарбо-новая кислоты-интенсивно-желто. [29]
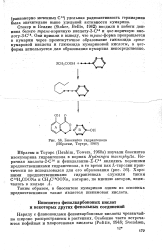 |
Биосинтез гидрангенола ( Ибрагим, Тоуэрс, 1960. [30] |
Страницы: 1 2 3 4