Хлорноватистая кислота
Cтраница 1
Хлорноватистая кислота присоединяется к цик-лопентену с образованием трамс-хлоргидрина. [1]
Хлорноватистая кислота обладает сильным окисляющим действием. [2]
Хлорноватистая кислота и ее соли являются весьма активными хлорирующими агентами, например, гипохлорит натрия способен хлорировать такие обычно инертные вещества, как хлороформ, бромоформ и йодоформ. [3]
Хлорноватистая кислота мало диссоциирована. [4]
Хлорноватистая кислота легко образует сложные эфиры со спиртами при низких температурах, а и присутствии олефипов дает хлорэфиры. Так, например, бснзосулъфодихлорадшд, который при гидролизе дает хлорноватистую кислоту, при подкислении в спиртовом растворе олефипа образует хлорэфяр. [5]
Хлорноватистая кислота НОС1 - очень слабая кислота ( К 5 - 10 - 8), более слабая, чем угольная; соли ее называются гипо-хлоритами. [6]
Хлорноватистая кислота - очень сильный окислитель; ее образованием при взаимодействии хлора с водой объясняются белящие свойства хлора. Совершенно сухой хлор не белит, но в присутствии влаги происходит быстрое разрушение красящих веществ образующейся при гидролизе хлора хлорноватистой кислотой. [7]
Хлорноватистая кислота из ее солей может быть вытеснена даже углекислым газом воздуха в присутствии воды. [8]
Хлорноватистая кислота в присутствии восстановителей отщепляет атомарный кислород, который может окислять H2S до элементарной серы. [9]
Хлорноватистая кислота существует только в водных растворах; в свободном состоянии она не получена, так как при обыкновенной температуре на свету постепенно разлагается. [10]
Хлорноватистая кислота - наиболее сильный окислитель, а гипо-хлорит-ион - наиболее слабый. [11]
Хлорноватистая кислота обладает высокой константой диссоциации, вследствие чего проблема подавления ионизации для нее практически не возникает. С, поэтому константу скорости реакции первого порядка можно резко изменять, добавляя относительно малые количества гипохлорита. Однако константа скорости сильно зависит от состава раствора и должна быть специально измерена для каждого используемого раствора абсорбента. Даже при соблюдении этого условия, в каждом случае необходима оценка того, не изменяется ли состав раствора у поверхности в ходе абсорбционного процесса, что отличало бы скорость реакции здесь от скорости в основной массе жидкости. [12]
Хлорноватистая кислота или бромная вода реагируют с изо-нреном с образованием моно - и дигалоидогидринов. [13]
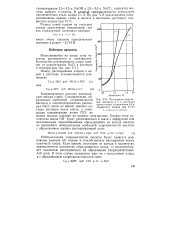 |
Потенциалы выделения водорода в 2 н. растворе едкого натра, содержащем 2 9 н. хлористого натрия при 75 С. [14] |
Хлорноватистая кислота диссоциирует весьма слабо. [15]
Страницы: 1 2 3 4