А-центр
Cтраница 2
Изменение спектра молекул СО2, адсорбированных модифицированной - фтором окисью алюминия, объясняется [30], как и в случае обработки НС1, изменением свойств а-центров. На рис. 119 представлен спектр СО2, адсорбированной на исходной и модифицированной фтором окиси алюминия. [16]
Как указано выше, наблюдая избирательную адсорбцию этих молекул алюмосиликагелями, Пери [20] предположил, что на поверхности существует особый тип центров адсорбции, так называемые а-центры. Пери считает, что эти центры образуются при удалении с поверхности гидроксиль-ных групп, связанных с поверхностными атомами алюминия алюмосиликагеля. Образование поверхностных гидроксильных групп при адсорбции НС1 дегидратированным и дегидроксилировэнным алюмосиликагелем указывает, по мнению Пери, на существование на поверхности реакционноспособного иона кислорода. Подобные состояния иона кислорода не имеют места на поверхности чистых кремнеземов. [17]
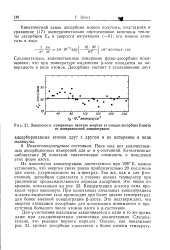 |
Зависимость измеренных величин энергии активации десорбции р-азота от поверхностной концентрации. [18] |
Из максимума концентрации, достигаемого при 298 К, можно установить, что энергия связи равна приблизительно 20 ккал / моль для азота, удерживаемого на а-центрах. Так же, как и для р-со-стояния, десорбция сдвигается в сторону низких температур при увеличении продолжительности периода адсорбции. Концентрация сс-азота сама проходит через максимум. При одинаковых начальных концентрациях а-азота выделение газа происходит при более низких температурах для более высокой концентрации р-азота. Это подтверждает, что энергия активации десорбции для ос-состояния понижается в присутствии большого числа атомов азота в ( 5-состоянии. [19]
Такие антибиотики, как норвалин и индолмицин, препятствуют образованию аминоацил-т РНК; стрептомицин, неомицин, конвалин, ауринтрикарбоновая кислота ингибируют инициацию трансляции; тетрациклин и стрептограмин ингибируют элонгацию, препятствуя связыванию аминоацил-т РНК с А-центром рибосомы. Пептидилтрансферазная реакция блокируется пуромицином и хлор-амфениколом, а транслокация - эритромицином и биомицином. [20]
Таким образом, в пептидильном центре локализуется формилметио-нин - тРНК, а в аминоацильном - тРНК, соединенная со следующей после ме-тионина аминокислотой. Следующим этапом элонгации является гидролиз сложноэфирной связи, перенос формилметионина из Р - центра в А-центр и образование пептидной связи. Этот процесс осуществляется при помощи фермента транспептид азы, входящей в состав 50S рибосомальной субъединицы. Находившаяся до этого в Р - центре тРНКШе1 отделяется от рибосомы и уходит в цитоплазму. Перемещение рибосомы по цепи мРНК происходит с помощью третьего фактора элонгации TF-G и требует затраты энергии ГТФ. Таким образом, завершается цикл элонгации, и белок-синтезирующая система готова к образованию следующей пептидной связи. [21]
Фракционированием освобожденного от клеток экстракта Bacillus breuis выделена синтетаза грамицидина С, состоящая из легкой и тяжелой фракций ферментной системы. Легкий фермент специфически активирует L-фенилаланин, получается соответствующий аденилат с переносом аминокислоты на тиольную группировку молекулы фермента, хиральный а-центр которой имеет D-конфигурацию. Хотя этот механизм не выяснен до конца, известна его независимость от коферментов и он, возможно, катализируется основаниями. [22]
Иными словами, это интервал ] а - б, з б [, из которого исключена точка а-центр интервала. [23]
Было показано, что в отличие от окиси алюминия фторирование или не изменяет свойств сильных кислотных центров ( а-центров, см. главу VIII), или приводит к их блокировке. Соответственно уменьшается активность этих катализаторов в реакции полимеризации бутилена. Спектры показывают, что обработка алюмосиликагеля NH4F при 600 С с последующей откачкой при 700 С, как и в случае окиси алюминия ( см. главу VIII), приводит к удалению всех гидроксильных групп. [24]
А-центр); и возможно, что для возбуждения рецептора необходимо, чтобы как А -, так и Б - центры были соединены с ацетилхолином. Если же антихолинэстеразный яд связывается с Б - центром рецептора, то добавленный потом ацетилхолин может реагировать только с А-центром. Для объяснения найденных явлений предполагается, что взаимодействие антихолинэстеразного яда с Б - центром рецептора обратимо, в то время как его реакция с Б - центром холинэсте-разы относительно необратима. [25]
Кроме того, центры окраски можно разделить на электрически нейтральные и заряженные по отношению к кристаллической решетке. К нейтральным центрам относятся F -, FA - и М - центры, а к заряженным - F - и а-центры. Заряженные центры обычно могут в кристалле существовать только попарно, взаимно компенсируя при этом свой электрический заряд. К таким парам, например, относятся F - и сс-центры. [26]
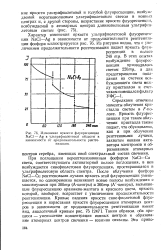 |
Изменение яркости флуоресценции NaCI - Ag в ультрафиолетовой области в зависимости от продолжительности рентгенизации. [27] |
При поглощении нерентгенизованным фосфором NaCI-Си света, соответствующего активаторной полосе поглощения, в нем возбуждается синефиолетовая флуоресценция, простирающаяся в ультрафиолетовую область спектра. После облучения фосфора NaCI-Си рентгеновыми лучами яркость этой флуоресценции уменьшается, но одновременно возникают новые полосы возбуждения с максимумами при 300т [ г ( А-центры) и 360 / П [ г ( А - центры), вызывающие флуоресценцию оранжево-желтого и красного цвета, яркость которой, наоборот, возрастает с увеличением продолжительности рентгенизации. Таким образом, оба процесса - уменьшение концентрации ионных центров и образование атомарных центров свечения - взаимно связаны. [28]
 |
Максимумы полос поглощения атомарных центров серебра и F-центров. [29] |
Следовательно, в щелочно-галоидных фосфорах указанные полосы обусловлены двумя различными видами атомарных центров. Оба вида атомарных центров отличаются между собой не только своими спектрами поглощения, но и по спектрам флуоресценции. Для А-центров в случае фосфоров NaCl - Ag характерна зеленая флуоресценция, тогда как для А - центров характерна флуоресценция оранжевого цвета. [30]
Страницы: 1 2 3