А-центр
Cтраница 3
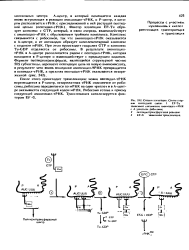 |
Стадии элонгации. Синтез первой пептидной связи. / EF-Tu зависимое связывание аминоацнч-т РНК с А участком рибосомы. [31] |
Фактор элонгации EF-Tu образует комплекс с GTP, который, в свою очередь, взаимодействует с аминоацил-т РНК с образованием тройного комплекса. При этом происходит гидролиз GTP и комплекс Tu-GDP отделяется от рибосомы. В результате аминоацил-т РНК в А-центре располагается рядом с пептидил-т РНК, которая находится в Р - центре и взаимодействует с предыдущим кодоном. [32]
Несмотря на двустадийный механизм, процесс, по-видимому, полностью стереоспецифичен. Более того, если лейцина дейтерирован аналогичным образом, дей-оказывается только в а - и р-центрах. В у-положении дей-нет, что указывает на отсутствие миграции двойной связи при восстановлении. Важное достоинство, присущее механизму - взаимообусловленность оптической чистоты f и а-центра. [33]
Легко подсчитать число макроэргов, которые расходуются на образование одной полипептидной связи. При активации аминокислот АТФ гидролизуется до АМФ, что эквивалентно затрате двух макроэргов, а инициация трансляции требует один макроэрг ГТФ. В процессе элонгации затрачивается два макроэрга ГТФ: один на доставку аминоацил-т РНК в А-центр рибосомы, а второй - на процесс транслокации. И наконец, на терминацию требуется один макро-эрг ГТФ. [34]
Механизм антибиотического действия тетрациклинов до настоящего времени окончательно ие установлен. Уже в 1950 г. было показано, что хлортетрациклин является специфическим ингибитором синтеза белка у Staphylococcus aureus. В настоящее время известно, что тетрациклины в присутствии иоиов калия и магния образуют прочные комплексы ( 1: 1) как с 70S рибосомами прокариотов, так и с 80S рибосомами эукариотов и полностью блокируют синтез белка. Конкретные мишени действия тетрациклинов - 30S и 40S субчастицы рибосом, а точнее - их участки акцепторного связывания аминоацил-т РНК ( А-центры) ( см. с. Взаимодействие тетрациклинов с рибосомами ( и полисомами) обратимо, и это обусловливает бактериостатический характер их активности. [35]
Процесс элонгации принято делить на 3 стадии: узнавание кодона и связывание аминоацил-т РНК, образование пептидной связи и транслокация. На I стадии в соответствии с природой кодона мРНК в свободный А-участок рибосомы доставляется аминоацил-т РНК при участии фактора элонгации Tu. Этот процесс требует затраты энергии и сопряжен с гидролизом ГТФ и образованием прочно связанного комплекса Tu-ГТФ. Образовавшийся комплекс подвергается диссоциации только в присутствии второго фактора элонгации Ts, при котором освободившийся фактор Tu может вновь, соединяясь с молекулой ГТФ, принять участие в доставке аа-т РНК в рибосому. С этого момента начинается II стадия элонгации-образование первой пептидной связи. Для этого в рибосоме осуществляется ферментативная реакция транспептидирования между формилметионил-т РНК в П - центре и новой аа-т РНК в А-центре. В процессе этой реакции остаток формилметионина переносится на свободную NH2 - rpynny аа-т РНК и замыкается первая пептидная связь в будущей полипептидной цепи. Параллельно из пеп-тидильного центра освобождается тРНК Мет в цитозоль. Фермент, катализирующий реакцию транспептирования, получил название пептидил-трансферазы ( рис. 14.7); он, вероятнее всего, является составной частью белков 50S субчастицы. [36]
Страницы: 1 2 3