Добавка - катион
Cтраница 1
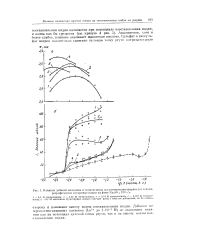 |
Влияние добавок мочоншш и тиомочовины на электрокашшлярпыс ( я и полярографические ( б кривые индия на фоле Na2SO4 190 г / л. [1] |
Добавки по-порхностно-активных катионов ( La3 до 1 - JO-3 М) не окапывают влияния как на потенциал пулевой точки ртути, так и на высоту волны восстановления индия. [2]
При добавке катионов благородных металлов в раствор наблюдаются характерные изменения стационарного потенциала металла в зависимости от вида катиона и его концентрации. В табл. 44 приведены значения потенциалов металлов, устанавливающихся по истечении 50 час. При сравнении стационарных потенциалов сплавов с потенциалами металла добавки в тех же условиях можно видеть, что потенциал сплава соответствует потенциалу металла добавки или даже превышает его. Последнее наблюдается для растворов, содержащих ионы меди. [3]
Результаты применения добавок катионов тяжелых металлов, обладающих, по мнению большинства авторов, каталитическими свойствами, весьма различны. Орнштепн и Круке 37, Ольценскпй у8 считают, что добавки меди и серебра, улучшают бактерицидный эффект хлорирования при малых концентрациях ионов этих металлов значительно сильнее, чем это могло бы иметь место при аддитивном суммировании бактерицидного эффекта каждого из этих веществ. [4]
Установлено, что концентрация добавки электроположительного катиона в коррозионный раствор будет зависеть от состояния поверхности защищаемого сплава и его основных пассивационных характеристик, которые можно иметь, например, на основании известных для данных условий анодных потенциостатических кривых. [5]
При образовании и-проводящих окислов и при добавках катионов с высшей валентностью для уменьшения концентрации дефектов необходимо знать, входят ли инородные катионы в окисел при максимальной валентности. Если они принимают ту же самую валентность, что и катионы основного окисла, то никакого изменения в концентрации дефектов не будет. [6]
Два основных метода уменьшения или предупреждения такой деградации заключаются в добавке катионов в носитель [6] и в использовании взаимодействия катализатора с носителем ( см. разд. [7]
На основании данных табл. 1 можно сделать общий вывод о том, что добавки катионов, вводимых в форме сульфатных соединений в количествах, эквивалентных 1 % H2SO4 от веса СгО3, мало сказываются на общих результатах электролиза и выходе по току. [8]
На рис. 81 показано, в качестве примера, влияние на электрокапиллярную кривую ртути добавки катиона таллия и комплексного катиона тетрабутиламмония. Адсорбция катионов смещает максимум электрокапиллярной кривой в сторону более положительных потенциалов. [9]
Если окалина является - проводником или проводником ионного типа с диффузией катионов по вакансиям или анионов в междоузлиях, то добавка катионов с более высокой валентностью к окалине снижает скорость окисления. Аналогичное снижение происходит, когда окалина является р-проводником или проводником ионного типа с диффузией анионов по вакансиям или катионов по междоузлиям с добавкой катионов с более низкой валентностью по отношению к окалине. В условиях, когда валентности обоих металлов равны, замена катионов основного металла катионами добавки не должна существенно влиять на интенсивность окисления. Эти правила, конечно, действительны при осуществлении объемной диффузии и теряют свою значимость, если превалирует диффузия по границам зерен или по поверхности. [10]
Парравано нашел, что при низких температурах энергия активации окисления СО не изменялась при переходе от чистого NiO к NiO с добавками катионов более низкой ( Ag, Li) или более высокой ( Cr, W) валентности. Низкотемпературный механизм не связан с электропроводностью и должен соответствовать весьма лабильной форме кислорода, по-видимому Оадс. Работы Стоуна [100] и его школы подтверждают это мнение. Выделяющаяся при этом энергия составляет 127 ккал / моль. Следовательно, при невысоких температурах комплекс не принимает участия в реакции и попросту отравляет большую часть поверхности. По-видимому, он образуется в результате реакции с ионизованным кислородом, в катализе же участвует лабильная форма Оадс. [11]
Применим теперь метод, описанный выше на примере окиси цинка, к окислению окиси углерода на закиси никеля, содержащей добавки обоих типов. Если окажется, что добавка катионов валентности выше и ниже двух воздействует на скорость каталитической реакции в противоположных направлениях, то можно будет сделать вывод о связи между каталитическими и полупроводниковыми свойствами вещества. [12]
Брегманом и Ньюменом [129, 130] было проведено исследование влияния добавок цинка и других катионов к комбинации, состоящей из полифосфата и ферроцианида. Они нашли, что добавки катионов кобальта, церия, хрома, марганца, кадмия, цинка и никеля оказывают положительное влияние. Катионы же урана, кремния, таллия, циркония, железа, меди, сурьмы, бериллия и алюминия, наоборот, снижают эффективность ингибиторов. С точки зрения стоимости и растворимости добавка цинка является практически наиболее приемлемой для использования в смешанных ингибиторах, применяемых в системах башенного охлаждения. Оптимальные составы получаются при введении цинка в количестве от 1 до 2 мг / л на 25 мг / л полифосфата. Берд [124] указывает на эффективность комбинированного состава из полифосфата и цинка. По сообщению Такеуши [98], как Zn, так и Ni улучшают ингибирующее действие гексаметафосфата. [13]
В этом процессе функцию катализаторов окисления и промоторов выполняет инертный пористый носитель. Вместе с тем в обоих процессах обязательна добавка катиона щелочного металла. [14]
При количествах осадителя, меньших эквивалента полианиона, также образуется стабильная суспензия. Настички приобретают отрицательный заряд и для их нейтрализации необходима добавка катионов высшей валентности. [15]
Страницы: 1 2 3