Колебание - молекула
Cтраница 1
Колебания молекул порождают полосы поглощения в инфракрасной области спектра, частоты которой можно измерить с помощью широко известных методов. Некоторые из этих колебаний, по-видимому, связаны с колебаниями отдельных связей. Так, например, соединения, содержащие карбонильную группу, обладают сильной характеристической полосой в области 1700 см-1. Поэтому изменения частоты соответствующей полосы поглощения в инфракрасном спектре могут рассматриваться как характеристика колебательной частоты связи и, следовательно, прочности связи. [1]
Колебания молекулы представляют собой периодические изменения конфигурации системы ядер. В отличие от поступательного движения и вращения, при которых молекула перемещается как целое, при колебаниях изменяется взаимное расположение ядер. Конфигурация колеблющейся молекулы в каждый момент времени характеризуется смещениями ядер из их равновесных положений. Геометрическому изучению колебаний молекул, иначе говоря изучению свойств смещенных конфигураций, должно естественно предшествовать рассмотрение свойств равновесной конфигурации, являющейся для колебаний исходной. Как при изучении равновесной конфигурации, так и при изучении смещенных конфигураций весьма существенен учет свойств симметрии. Со свойствами симметрии равновесной конфигурации связаны и свойства симметрии смещенных конфигураций. [2]
Колебания молекул могут менять как взаимные расстояния между ближайшими атомами, так и углы между направлениями валентностей. Например, в молекуле СО2, имеющей прямолинейную равновесную форму О-С - О, существуют колебания, при которых изменяются расстояния между ядрами О и С, а также другие колебания, выводящие ядро С из прямолинейного расположения. Первый тип колебаний называется валентным, второй - деформационным. [3]
Колебания молекул включают такое большое количество протонного взаимодействия, что относительное вращение колец добавляет к этому слишком мало; поэтому становится невозможным провести различие между этими двумя видами движения. [4]
Колебания молекул предполагаются малыми и гармоническими. Следовательно, в принятом приближении все преобразования между различными координатами смещений линейны и их удобно представить в матричном виде. [5]
Колебания молекулы, обладающей п колебательными степенями свободы, описываются при помощи п нормальных колебаний, каждое из которых ( в гармоническом приближении) не зависит от остальных колебаний. [6]
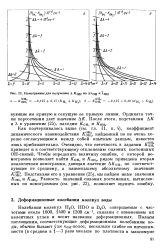 |
Номограммы для получения Д ЛТдн по. [7] |
Колебания молекул Н2О, HDO и D2O, совершаемые с частотами около 1600, 1400 и 1200 см 1, связаны с изменением их валентных углов и носят название деформационных. [8]
Колебания молекулы НаО, ассоциированной с молекулой А по схеме I, должны существенно измениться по сравнению с колебаниями изолированной молекулы ШОв инертном растворителе. [9]
Колебаниям молекул также соответствует дискретный набор состояний и тем самым дискретный набор энергетических уровней. Для строгого решения задачи о колебательных состояниях молекулы нужно знать для каждого колебания функцию U ( R), описывающую кривую потенциальной энергии соответствующей химической связи. Однако даже для двухатомной частицы эта функция может быть найдена только путем сложных квантово-механических расчетов и не описывается каким-либо аналитическим выражением. [10]
Колебаниям молекул также соответствует дискретный набор состояний и тем самым дискретный набор энергетических уровней. Для строгого решения задачи о колебательных состояниях молекулы нужно знать для каждого колебания функцию U ( R), описывающую кривую потенциальной энергии соответствующей химической связи. Однако даже для двухатомной частицы эта функция может быть найдена только путем сложных квантовомеханических расчетов и не описывается каким-либо аналитическим выражением. [11]
Колебаниям молекул также соответствует дискретный набор состояний и тем самым дискретный набор энергетических уровней. Для строгого решения задачи о колебательных состояниях молекулы нужно знать для каждого колебания функцию U ( R), описывающую кривую потенциальной энергии соответствующей химической связи. Однако даже для двухатомной частицы эта функция может быть найдена только путем сложных квантовомеханических расчетов и не описывается каким-либо аналитическим выражением. [12]
Колебаниям молекул также соответствует дискретный набор состояний и тем самым дискретный набор энергетических уровней. Для строгого решения задачи о колебательных состояниях молекулы нужно знать для каждого колебания функцию U ( R), описывающую кривую потенциальной энергии соответствующей химической связи. Однако даже для двухатомной частицы эта функция может быть найдена только путем сложных квантово-механических расчетов и не описывается каким-либо аналитическим выражением. [13]
Если колебания молекулы активны как в спектре комбинационного рассеяния, так и в ИК-спектре, то между этими спектрами существует заметная корреляция. Однако интенсивности наблюдаемых полос в этих двух спектрах часто бывают различными. Обычно большинство колебаний, обусловливающих интенсивные ИК-полосы поглощения, не дают сильных полос в спектрах комбинационного рассеяния. И наоборот, сильные полосы в спектрах комбинационного рассеяния обычно возникают в результате колебаний молекулы, которые генерируют слабые ИК-сигналы. Например, валентные колебания ОН-групп, которые сильно проявляются в ИК-спектре, дают относительно слабый пик в-спектре комбинационного рассеяния. В отличие от этого, колебания S-S - связи наблюдаются в спектре комбинационного рассеяния, но не проявляются вообще в ИК-спектре. Высоко симметричные колебания, такие как колебания СС - и С С-связей, сильно проявляются в спектре комбинационного рассеяния, что делает СКР особенно важной для-изучения колебаний скелета органических молекул. Колебания полярных групп активны в ИК-спектре, поэтому ИК-спектрометрия имеет особое значение для идентификации заместителей в органических молекулах. [14]
Когда колебания молекулы относительно положения равновесия станут большими ( например, при нагревании), то молекула может перейти от одной группы молекул к другой. В этом случае возможен фазовый переход и состояние тела станет жидким. Измерения рентгеновских лучей, проходящих через жидкости и твердые тела, показывают, что в жидкости молекулярная система менее правильна. [15]
Страницы: 1 2 3 4