Добавка - пиридин
Cтраница 1
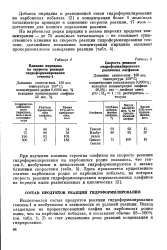 |
Скорость реакции гидроформилирования различных олефинов. [1] |
Добавка пиридина к реакционной смеси гидроформилирования на карбонилах кобальта [2] в концентрации более 1 моль / моль катализатора приводит к снижению скорости реакции, 17 моль - достаточно для полного подавления реакции. [2]
Добавка пиридина значительно увеличивает выход линейного аналога. [3]
Добавки пиридина, диоксана и ТГФ не разрушают этот комплекс. Известны и другие металлоциклические соединения. [4]
Добавка пиридина [176, 180] и особенно имидазола и имида-зольных производных [194] к ге-мину усиливает его пероксидазное действие ( см. табл. 10 и 11, методика - стр. [5]
При добавке пиридина вращение также не обнаружено. Изменения, которые при этом возникают, были истолкованы как я - сг-переход, начинающийся синхронно с присоединением молекулы пиридина. [6]
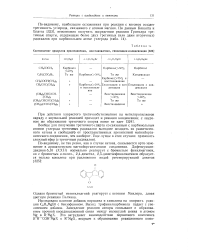 |
Соотношение продуктов присоединения, восстановления, енолизации и конденсации. [7] |
Исследовано влияние добавок пиридина и хинолина на скорость реакции C6H5MgBr с бензофеноном. Выход трифенилкарбинола падает с увеличением добавок. [8]
Реакция ускоряется добавкой пиридина, иода. [9]
Анантакришнан нашел, что добавка пиридина не изменяет скорости реакции. Если бы реакция проходила по схеме Вестгей-мера с промежуточным образованием эфира ( 2), прибавление пиридина должно было увеличивать скорость отрыва протона. [10]
Степень ускорения, вызываемого добавкой пиридина, определяется структурой олефина. Так, для пропилена, изобутилена и циклогексена ( табл. 1 и 5) в присутствии пиридина реакция ускоряется в 1 5 - 3 раза. [11]
Недавно было установлено [20], что добавка пиридина заметно ускоряет реакцию синтеза кислот из олефинов, окиси углерода и воды. Представлялось интересным изучить влияние пиридина на скорость реакции получения эфиров из олефинов, окиси углерода и спирта. [12]
 |
Установка непрерывного адсорбционного разделения газов ( гиперсорбции Института промышленных исследований Японии ( Ш1. [13] |
Ингибирующее действие также оказывали 0 01 - 1 % добавки пиридина и алкилпиридинов, 0 01 - 5 % морфолина или алкилморфолинов, К. В растворе N-метилпирролидона заметный ингибирующий эффект вызывали добавки 0 5 % хинона, гидразина, красителя метиленового синего, нитрофенолов, гексамети-лентетрамина, алканоламинов. [14]
Шоппи [183] показал, что холестерин при действии пятихлористого фосфора и тионилхлорида ( с добавкой пиридина или без него) превращается в холе-стерилхлорид с сохранением конфигурации в месте замещения. Механизм этих реакций, несомненно, близок к механизму гидролиза хлорида, который, как уже отмечалось, протекает с сохранением конфигурации. Это служит дополнительным доказательством того, что двойная связь в холестерине способствует сохранению конфигурации. [15]
Страницы: 1 2 3