Количество - поглощенный кислород
Cтраница 2
Количество поглощенного кислорода будет сложным образом зависеть от скорости поступления газа и от всех других переменных, входящих в уравнения, которые описывают перемещение фаз. Определить точный вид зависимости между скоростью подачи газа и другими переменными практически невозможно; однако анализ размерностей позволяет установить ряд важных соотношений, которые должны выполняться для любой такой зависимости. Это связано с тем, что корректные способы измерений удовлетворяют требованию, согласно которому число, равное отношению между результатами измерений двух объектов, не зависит от того, какая единица используется для измерений, а корректные системы уравнений, имеют такой, вид, который не зависит от системы единиц. [16]
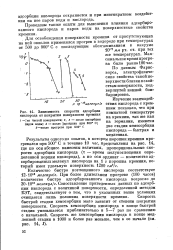 |
Зависимость скорости адсорбции кислорода от покрытия поверхности кремния. [17] |
Количество быстро поглощенного кислорода соответствует 12 - Ю16 молекул / г. При более длительном прогреве ( 100 часов) количество быстро адсорбированного кислорода возросло до 20 - Ю16 молекул / г. Сопоставление приведенных данных по адсорбции кислорода с величиной поверхности, определенной методом БЭТ, свидетельствует о том, что в указанных выше условиях очищается лишь половина поверхности кремния. Скорость быстрой стадии хемосорбции мало зависит от степени покрытия поверхности. Скорость хемосорбции кислорода в конце быстрой стадии уменьшается приблизительно в 5 - 7 раз по сравнению с начальной. [18]
Но количество поглощенного кислорода не превышает 20 % от содержащегося в воздухе, подаваемом на окисление. [19]
Почему количество поглощенного кислорода во много раз превышает то, которое требуется для полного окисления добавленного оксалоацетата или малата. [20]
Увелиаение количества поглощенного кислорода с понижением температуры не может быть связано с появлением физической адсорбции, так как наблюдаемое поглощение кислорода платиной необратимо. Кислород, адсорбированный в этих условиях на силикагеле, легко удаляется откачкой. Одной из существенных особенностей низкотемпературной формы хемосорбции является сравнительно небольшая энергия активации. Хемосорбция О2 на Pt при - 130 и - 150 С заканчивается менее чем за 5 мин. [21]
Определение количества поглощенного кислорода при фотохимическом окислении гексациклогексилдисвинца в бензоле показало, что 1 моль исходного свинецорганнче-ского соединения поглощает около 1 3 моля кислорода. [22]
Поэтому изменение количества поглощенного кислорода в нефтепродуктах будет зависеть в основном от количества кислорода, содержащегося в газовом пространстве, и частоты заполнения и опорожнения технических средств, в результате которых паровое пространство и самый продукт обогащаются кислородом, а также осуществляется лучший контакт кислорода с корродируемой поверхностью. [24]
Связь между количеством поглощенного кислорода и изменением эксплуатационных свойств резин является, по-видимому, весьма сложной и может изменяться с температурой. Имеющийся экспериментальный материал еще недостаточен для окончатель ных выводов. [25]
Связь между количеством поглощенного кислорода и изменением эксплуатационных свойств резин является, по-видимому, весьма сложной и может изменяться с температурой. Имеющийся экспериментальный материал еще недостаточен для окончательных выводов. [26]
По мере увеличения количества поглощенного кислорода также непрерывно изменяется коэффициент преломления. [27]
Сопоставление данных по количеству поглощенного кислорода показывает, что защитные свойства покрытий зависят не только от их состава, но и от защищаемого материала. Предварительно закрепленные обжигом на воздухе покрытия на всех сплавах поглощают значительно меньше кислорода ( 3.5 - 2.0 вес. [28]
Скорость увеличивается пропорционально количеству поглощенного кислорода по крайней мере до поглощения 0 2 моля кислорода на молекулу олефина; при более высоких степенях превращения такое ускорение не наблюдается. Однако кинетические исследования были ограничены начальной стадией реакции. То, что реакция инициируется в результате распада гидроперекисей, было подтверждено корреляцией скоростей окисления и распада гидроперекисей. Небольшие, но конечные скорости в начале реакции при окислении вещества, не содержащего перекисей, будут рассмотрены на стр. [29]
Опыты оценивали по количеству поглощенного кислорода и содержанию в оксидате продуктов окисления - циклооктилгиропероксид анализировали иодометричсски, циклооктанол и циклооктанон - хроматографически после предварительного восстановления анализируемой пробы трифенилфосфином [12]; кислоты - потенциометрическим титрованием раствором щелочи. [30]
Страницы: 1 2 3 4 5
