Количество - сильная кислота
Cтраница 1
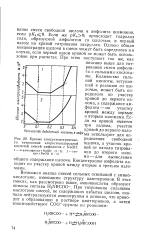 |
Кривые кондуктометрическо - РеДеления свободной го титрования хлористоводородной кислотой смесей амфолитов с NaOH. [1] |
Количество сильной кислоты, вступившей в реакцию со щелочью, может быть определено по участку кривой до первого излома, а содержание амфолита - по участку кривой между первым и вторым изломами. [2]
Вычисление количества сильной кислоты, которое следует добавить к данному раствору слабой кислоты, чтобы снизить до заданной величины концентрацию аниона. [3]
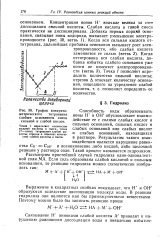 |
График кондукто. [4] |
Точка / определяет количество сильной кислоты в смеси, точка II - конец титрования слабой кислоты; отрезок Д отвечает количеству слабой кислоты в смеси. [5]
Буферная емкость определяется количеством сильной кислоты или сильного основания, которые при добавлении в буферную систему изменяют на единицу значение рН одного литра буферного раствора. [6]
 |
Константы диссоциации некоторых слабых оснований при 25 С. [7] |
При добавлении в воду некоторого количества сильной кислоты наблюдается такой же эффект, как при добавлении того же количества ионов водорода, так как кислота полностью диссоциирует. [8]
Добавим к полученному раствору некоторое количество сильной кислоты ( например, НС1), которое, однако, должно быть незначительным по сравнению с имеющимся в растворе количеством слабой кислоты и ее соли. [9]
Если ввести в раствор некоторое количество сильной кислоты, которая полностью ионизуется, то концентрация ионов водорода будет равна концентрации кислоты. [10]
В связи с тем, что количество сильной кислоты ( как катализатора) остается неизменным, увеличение количества щелочи, идущей на титрование отбираемых проб реагирующей смеси. [11]
Если к раствору многоосновной кислоты добавить некоторое количество сильной кислоты, то возникающее при этом резкое увеличение концентрации ионов Н приводит к значительному уменьшению концентраций других ионов, образующих равновесную систему. [12]
Реакция карболовой кислоты и спирта в присутствии ледовых количеств сильной кислоты, в результате которой образуются сложный эфир и вода. Для того чтобы реакция шла до конца, либо добавляют избыток кислоты ( или спирта), либо удаляют воду по мере ее образования. [13]
Если к раствору слабой многоосновной кислоты добавить некоторое количество сильной кислоты, то возникающее при этом резкое увеличение концентрации ионов Н приводит к значительному уменьшению концентраций других ионов, образующих равновесную систему. [14]
При вычислении ионного состава раствора многоосновной кислоты, содержащего некоторое количество сильной кислоты, принимают, что концентрация ионов Н практически зависит только от концентрации сильной кислоты, а концентрация ионов Н, образующихся в результате диссоциации многоосновной кислоты, столь незначительна, что ею можно пренебречь. [15]
Страницы: 1 2 3