Простые амин
Cтраница 1
Простые амины также являются продуктами разложения органических веществ, содержащих азот. [1]
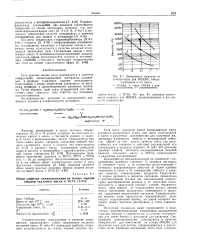 |
Зависимость вязкости от температуры для DGEBA, амидополиамина и их смеси. / - - DGEBA. 2 - смесь DGEBA с ами-дополиамином. 3 - амидополиамин. [2] |
Хотя простые амины мало используются - в качестве отвердителей, аминосодержащие материалы, называемые в продаже амидами, широко используются. Отверждение с этими веществами достигается не амид-ными группами, а присутствующими аминными группами. Таким образом, один класс отвердителей для эпоксидных смол амидного типа известен под названием амидополиаминов. [3]
Названия простых аминов строятся по алкильным или арильным группам связанным с азотом. Анилин - тривиальное наименование простейшего ароматического амина ( C6H6NH2); если углеводородная или какая-либо функциональная группа соединена с бензольным циклом анилина, то эти вещества можно называть как производные анилина. Гетероциклические соединения с азотом в качестве компонента циклической системы обычно носят особые названия, иногда в зависимости от их структуры. [4]
Основность простых аминов определяется электроноакцепторным ( О N Н) или электронодонорным ( С Н) эффектом заместителей. Это приводит соответственно к уменьшению или увеличению стабильности положительно заряженной кислоты и, следовательно, к возрастанию или уменьшению ее кислотности. [5]
 |
Структура аминов и ионов четвертичного аммония. [6] |
Названия простых аминов строятся по алкильным или арильным группам, связанным с азотом. Анилин - тривиальное наименование простейшего ароматического амина ( C6H5NH2); если углеводородная или какая-либо функциональная группа соединена с бензольным циклом анилина, то эти вещества можно называть как производные анилина. Гетероциклические соединения с азотом в качестве компонента циклической системы обычно носят особые названия, иногда в зависимости от их структуры. [7]
Окисление простых аминов и фпнолов. В том tijysac, к01 Да амин илл фенол лето доступны или когда нужно получить лишь небольшое количестно хинона, часто наиболее удобно проводить прямое окисление, не прибегая к виедению заместителя в пара-положение к амино - и ии гидроксилытп группе. [8]
Исследование спектров простых аминов в вакуумной ультрафиолетовой области показывает, что расширение практически применяемого УФ-диапазона в эту область спектра позволяет получить ценный метод идентификации первичных, вторичных и третичных алифатических аминов. [9]
Общепринято, что у простых аминов частота внутренних деформационных колебаний NH2 составляет 1650 - 1590 слг1, но этот интервал был установлен в результате исследований очень небольшого числа соединений, а именно метиламина [8, 9], анилина [10-12], гидразина [18] и замещенных гидразина [36], причем каких-либо более общих исследований не проводилось. Имеется, однако, значительно больше данных о простых амидах, у которых частоты деформационных колебаний NH2 находятся в этой же области и хорошо изучены многими авторами ( см. гл. Эти данные косвенным образрм свидетельствуют о правильности такого отнесения частот, однако некоторые авторы высказывают сомнение в отношении того, является ли вообще соответствующая полоса поглощения вторичных амидов связанной с деформационными колебаниями NH. Работы с дейтерированными соединениями подтверждают ту точку зрения, что поглощение в указанной области у первичных амидов и аминов обусловлено деформационными колебаниями NH; для аминов наблюдается также смещение некоторых полос поглощения в более длинноволновую часть спектра. Однако полоса поглощелия в интервале 1650 - 1590 см-1 имеется почти во всех спектрах первичных аминов, сведения о которых нам удалось найти в литературе, а также у значительного числа таких веществ, исследованных нами. [10]
Разрыв связей алкильной цепи частично напоминает распад простых аминов ( см. разд. Процессы а -, Р - и уразрывов, интенсивность которых уменьшается - в ряду оС р У - вызьГ ат 1Го вл 1ше - - вГсп - ектре пиков с т / е 80 ( л), 94 и 108 соответственно. Действительно, пик образовавшегося при этом иона пиррола I ( т / е 67) имеет заметную величину, хотя положение, из которого мигрирует водородный атом, неизвестно и должно быть еще установлено с помощью метки дейтерием. [11]
Из азотистых соединений в нефтях обнаружены аммиак, простые амины, пиридин и хинолин. Низшие амины хорошо растворимы в воде. Например, при 12 С в воде растворяется 1150 объемов метиламина. Пиридин имеет удельный вес 0 98, температуру плавления 42 С, температуру кипения 115 4 С, в воде растворим в любых количествах. Таким образом, в воде азотистые соединения находятся или в виде газа, или в виде жидкости. [12]
В некоторых нефтях в весьма незначительных количествах могут содержаться также простые амины и аммиак. [13]
В этом разделе рассматриваются методы получения, свойства и реакции простых аминов, содержащих аллильную группировку, например аллиламина ( 55), который является характерным представителем этого класса соединений. [14]
Гуанидины и ампдины представляют собой гораздо более сильные органические основания, чем простые амины. [15]
Страницы: 1 2 3