Количество - превращенное вещество
Cтраница 2
Выражение ( VII, 9) устанавливает для рассматриваемой реакции зависимость объема реактора от величины загрузки сырьем и количества превращенного вещества. [16]
Кинетика ферментативных процессов [18] также, как известно, часто уклоняется от закона действия масс в том смысле, что количества превращенного вещества пропорциональны лишь времени. [17]
При этих условиях, уже заведомо исключающих всякое влияние выделяющегося при реакции тепла, характерное течение реакции осталось - ц здесь количество превращенного вещества пропорционально лишь времени и не зависит от массы находящегося налицо вещества. Вопреки закону масс, количества вещества, подвергшегося превращению в равные промежутки времени, не только не уменьшаются, по, наоборот, даже несколько увеличиваются. Необходимо заметить, однако, что так как опыт при 0 шел в присутствии большого количества катализатора, то картина изменения объема жидкости отчасти зависела от различного расширения фосфористого и изомеризованного эфира с йодистым этилом. Влияние это, впрочем, как я упоминал, не могло сильно исказить характер основного процесса. [18]
Если при данной величине поверхности катализатора и произвольном времени пребывания изменить время работы установки, то очевидно, что пропорционально ему изменится количество превращенного вещества. [19]
Скорость реакции обозначается через со ( или v), и если время измеряется в секундах, объем в миллилитрах, а количество превращенного вещества в молях, то ее размерность равна моль / с-мл. [20]
Поскольку в гетерогенно-каталитических процессах величину объема катализатора V с учетом доли свободного объема определить с достаточной точностью гораздо труднее, чем его массу, в практике кинетических исследований часто количество превращенного вещества относят не к объему катализатора, а к его массе. [21]
Общая активность катализатора выражается глубиной превращения, а избирательность катализатора - величиной D - f - L и в особенности разностью между значениями D - f - L и количеством превращенного вещества. [22]
Скорость циркуляции намного больше скорости протока вещества через установку, что обеспечивает эффективное перемешивание и значительное превращение реагентов несмотря на использование дифференциального реактора. Количество превращенного вещества определяется по изменению состава подаваемой и выходящей из установки смесей. Как и для дифференциального проточного реактора, здесь применимы уравнения кинетики в дифференциальной форме. Таким образом, проточно-циркуляционный метод обладает преимуществами дифференциального проточного метода, но лишен его недостатков. [23]
К концу 1 - й минуты пероксидаза сохраняет еще во всех случаях свою полную активность. Количество превращенного вещества в точности пропорционально количеству пероксидазы в пределах ошибок опыта: функция от концентрации выражается прямой. К концу 2 - й минуты пропорциональность наблюдается только при концентрациях А - Е, к концу 3 - й минуты только при А-С, к концу 4 - й минуты только при А-В. [24]
 |
Кинетические кривые реакции гидрирования карбида железа водородом Рв2С 2Н2 2Fe CH4 при 300 С ( цифры на кривых - давление водорода ( по данным В. Д. Стыценко, А. Я - Розовского. [25] |
Как видно, наблюдаемая скорость реакции в начале процесса весьма мала, далее возрастает во времени, проходит через максимум и снижается до относительно малых значений. Интегральная кинетическая кривая ( зависимость количества превращенного вещества или степени превращения от времени) имеет характерную 5-образную форму. В соответствии с видом кинетических кривых различают индукционный период, период роста скорости, максимум скорости реакции и период ее снижения. [26]
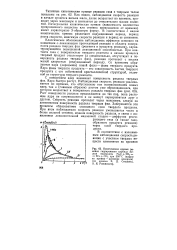 |
Кинетические кривые реакции гидрирования карбида железа водородом Fe2C 2Н2 2Fe CH4 при 300 С ( цифры на кривых - давление водорода ( по данным В. Д. Стыценко, А. Я. Розовского. [27] |
Как видно, наблюдаемая скорость реакции в начале процесса весьма мала, далее возрастает во времени, проходит через максимум и снижается до относительно малых значений. Интегральная кинетическая кривая ( зависимость количества превращенного вещества или степени превращения от времени) имеет характерную 5-образную форму. В соответствии с видом кинетических кривых различают индукционный период, период роста скорости, максимум скорости реакции и период ее снижения. [28]
Во всех рассмотренных случаях мы принимали, что свойства каталитической поверхности остаются неизменными и задавались определенным временем работы установки ( 1 мин. Вследствие этого во всех рассмотренных случаях одинаково и количество превращенного вещества. [29]
Знание теплового эффекта реакции необходимо для определения тепловых явлений в технологических процессах. Количество выделившейся ( или поглощенной) теплоты q зависит от количества превращенного вещества ДУУ. [30]
Страницы: 1 2 3