Небольшое количество - бензойная кислота
Cтраница 1
Небольшие количества бензойной кислоты могут конъюгировать с глюкуроновой кислотой и выводиться с мочой в виде бензоил-глюкуроновой кислоты. [1]
В одну пробирку помещают небольшое количество бензойной кислоты, в другую - 1 мл смеси нефтяных кислот. [2]
При щелочном расщеплении дракорубина образуется ацетофенон и небольшое количество бензойной кислоты ( образующейся из аце-тофенона) в качестве единственных идентифицированных веществ. Окисление щелочным раствором перекиси водорода приводит к разрыву пиранольного Кольца и образованию оптически активного двухатомного фенола, драконола ( IV, R Н), содержащего, так же как и дракорубин, трудно обнаруживаемую метоксильную группу, на что не обратили внимания немецкие исследователи. Метилирование 1379 ] этого фенола дает О-метилдраконол ( IV, R СН3), идентичный продукту, полученному вместе с ацетофеноном при щелочном расщеплении О-метилдракорубанола. [3]
С водяными парами при этом перегоняются маслянистые желтые капли и небольшое количество бензойной кислоты, оседающей в трубке холодильника и оказывающейся также в водном слое. Верхний слой перегона с водой разбавляют этиловым эфиром, промывают раствором соды, затем водой, высушивают плавленой сернонат-риевой солью; эфир отгоняют, маслянистый продукт перегоняют. [4]
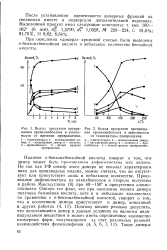 |
Выход продуктов превра - [ IMAGE ] Выход продуктов превраще-щения пропенилбензола в зависи - ния пропенилбензола в зависимости мости от времени превращения. от температуры превращения. [5] |
При окислении димера хромовой смесью были выделены о-бензоилбензойная кислота и небольшое количество бензойной кислоты. [6]
В продуктах озонолиза обнаружен бензил ( в большом количестве) и небольшое количество бензойной кислоты, которая, по-видимому, является продуктом оюислеиия бензила. [7]
Иногда при араминировании, в особенности красителей, вводят в реакционную смесь небольшое количество бензойной кислоты. [8]
При обработке стирола перманганатом калия при 70 образуется бензоилмуравьиная кислота вместе с небольшим количеством бензойной кислоты. [9]
В 1931 г. Кинни и Ланглуа [101] сообщили о том, что им удалось получить небольшое количество бензойной кислоты ( 0 13 % от веса исходного бензола) при нагревании бензола и углекислоты в течение 10 час. Однако четыре года спустя Кинни и Боннер [102] провели термодинамический расчет реакции С6Н6 С02 С6Н6СООН и пришли к выводу, что результаты предыдущей работы [101] были ошибочными. [10]
В 1931 г. Кинни и Ланглуа [22] сообщили о том, что им удалось получить небольшое количество бензойной кислоты ( 0 13 % от веса исходного бензола) при нагревании бензола и углекислоты в течение 10 ч при 300 С и 35 атм в присутствии катализатора, содержащего окислы цинка, меди и хрома. [11]
Если вышеописанный опыт вести так, чтобы нагревание шло не слишком быстро и не слишком сильно, к полученному телу каждый раз бывает примешано небольшое количество бензойной кислоты. Нерастворимая в аммиаке часть оказалась иглообразным телом вместе с небольшим количеством масла, обладающего запахом бензильного алкоголя. [12]
К небольшому количеству бензойной кислоты в пробирке прибавляют воду. Убедившись, что кислота не растворяется, добавляют по каплям крепкий раствор щелочи, пока кислота не растворится. После этого подкисляют раствор соляной кислотой. [13]
Затем бензойную кислоту экстрагируют эфиром в течение 1 часа, экстракт упаривают досуха и бензойную кислоту растворяют при 75 С в 75 мл воды. При охлаждении выпадает небольшое количество захваченной бензойной кислоты, которая отделяется. Отбирают определенную часть фильтрата, смешивают с 10 мл 1 N серной кислоты и разбавляют до 100 мл водой. [14]
Арилирование аминогрупп в молекуле Парарозанилина углубляет цвет до голубого. Осуществляют реакцию нагреванием Парарозанилина с избытком ароматического амина при кипении в присутствии небольшого количества бензойной кислоты. Избыток амина затем отгоняют в вакууме. [15]
Страницы: 1 2