Добавление - катион
Cтраница 1
Добавление проникающих синтетических катионов к митохондриям вызывает увеличение концентрации Н4 в среде. Изменения рН исчезают при добавлении разобщителей. При работе дыхательной цепи среда подкисляется. [1]
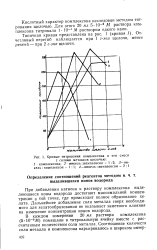 |
Кривые титрования комплексона и его смеси. [2] |
При добавлении катиона к раствору комплексона выделяющиеся ионы водорода достигают максимальной концентрации в той точке, где происходит полное образование хе-лата. Дальнейшее добавление соли металла сверх необходимого для хелатообразования не оказывает заметного влияния на изменение концентрации ионов водорода. [3]
Вследствие этого добавление одноименного катиона не влияет на природу поверхности и характер контактов частиц, рентгенографическая картина этих образцов не изменяется. [4]
Равновесие довольно подвижно, и при добавлении катионов, образующих нерастворимые хроматы, выпадают в осадок не бихроматы, а хроматы. Большое значение имеет также характер кислоты. [5]
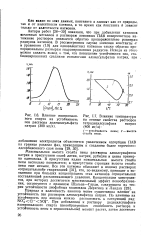 |
Влияние изопропило-вого спирта на устойчивость пен раствора додецилсульфата натрия ( 300 мг / л.| Влияние температуры на пенные свойства растворов тетрадецилсульфата натрия ( 400 мг / л. [6] |
Авторы работ [28-30] показали, что при добавлении катионов щелочных металлов к растворам анионных ПАВ поверхностное натяжение растворов снижается обратно пропорционально размерам радиусов катионов. В рассмотренном случае значения константы а в уравнении (1.9) для одновалентных катионов также обратно пропорциональны размерам гидратированных радиусов. [7]
 |
Строение бихромат-иона, установленное для соли. [8] |
Положение равновесия зависит от рН, и при добавлении катионов, которые образуют нерастворимые хроматы, например Ва2, РЬ2, Ag, осаждаются хроматы, а не бихроматы. Только для HNO3 и Н С1О4 имеют место равновесия, приведенные выше. [9]
Значение металла как комплексообразователя вытекает из того, что добавление катиона того же самого металла в виде какой-либо соли повышает эффективность соответствующей гидроокиси. [10]
В случае восстановления платинат-анионов i - / - кривые при добавлении поверхностноактивных катионов - имели еще более сложную форму, чем это наблюдалось в растворах персульфата или феррицианида. Кривые i - t подобной же формы можно наблюдать и в случае восстановления катионов ( например, [ Co ( NH3) e ] 3) в присутствии поверхностноактивных анионов [118]; например, таких, как высшие гомологи сульфоновых кислот. [11]
В случае восстановления платинат-анионов i - / - кривые при добавлении поверхностноактивных катионов имели еще более сложную форму, чем это наблюдалось в растворах персульфата или феррицианида. Кривые i - t подобной же формы можно наблюдать и в случае восстановления катионов ( например, [ Co ( NH3) 6 ] 3) в присутствии поверхностноактивных анионов [118]; например, таких, как высшие гомологи сульфоновых кислот. [12]
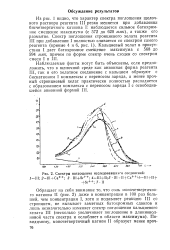 |
Спектры поглощения исследовавшихгя соединений. / Ш. 2 - Ш Са. 3 IIl Sr. 4 - ll ll. 5 - III U - - Ca 6 - l f II. [13] |
Из рис. 1 видно, что характер спектра поглощения щелочного раствора реагента III резко меняется при добавлении бисчетвертичного катиона I: наблюдается сильное батохром-ное смещение максимума ( с 572 до 620 ммк), а также его размытие. [14]
Заметим, что замещение ионов кислорода ионами меньшего отрицательного заряда ( например, С1 -) с точки зрения проводимости эквивалентно добавлению катионов с положительным зарядом, большим двух. [15]
Страницы: 1 2