Добавление - катион
Cтраница 2
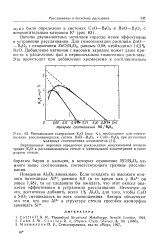 |
Минимальное содержание К2О ( мол. %, необходимое для гомогенизации расслаивающихся систем ВаО - В2О3 и СаО - В2О3 при различных. [16] |
Окислы двухвалентных металлов гораздо менее эффективны в устранении расслаивания. Добавление катионов с высоким зарядом может даже привести-к разделению фаз в первоначально гомогенном расплаве. [17]
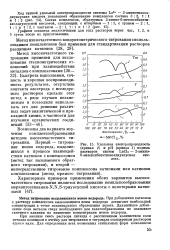 |
Удельная электропроводность ( кривая 2 и рН ( кривая 1 водных растворов систем LnCls - 2-амино - 6-метоксибензтиазолдиуксусная кислота. [18] |
При добавлении катионов к раствору комплексона выделяющиеся ионы водорода достигают наибольшей концентрации в точке максимального образования хелата. Дальнейшее добавление соли металла сверх необходимого для хелатообразования не оказывает заметного влияния на изменение концентрации ионов водорода. [19]
Некоторые препараты глутаминаз могут также осуществлять реакции переноса с участием гидроксиламина, приводящие к образованию f - глутамилгидроксамовой кислоты и аммиака. Эти реакции протекают без добавления катионов и нуклеотидов и в этом отношении отличаются от реакций переноса f - глутамила, протекающих при участии ферментов, синтезирующих глутамин ( стр. Вэлш и сотрудники [89, 90] нашли, что экстракты Proteus vulgaris катализируют обмен № 5-аммиака с амидными группами глутамина и аспарагина, а также образование 7-глут-амилгидроксамовой и р-аспартил-гидроксамовой кислот из гидроксиламина и со-амидов а-аминокислот. Очевидно, гидроксиламин может заменять природный субстрат. [20]
При высоких температурах в атмосфере кислорода наблюдается увеличение в размерах палладиевых кристаллитов, нанесенных на алюмосиликат, тогда как в водороде имеет место только отжиг дефектов кристаллической решетки с результирующей потерей удельной каталитической активности, а не поверхности. Также найдено, что добавление высоковалентного катиона ( например Th4, La3) увеличивает термическую стабильность - эффект, который, по-видимому, обусловливается затруднением поверхностной подвижности палладия из-за усиленного взаимодействия металл - носитель. [21]
Разница заключается лишь в том, что атомы Li и Fe заполняют больший процент кислородных октаэдров, возникающих между вольфраматными цепочками. Отличие этой структуры от LiaFe2 - ( Мо04) 3 можно представить как признак некоторого различия Мо и W в их склонности к октаэдрической координации: в молибдате добавление катиона щелочного металла ослабляет действие переходного металла ( Fe) настолько, что координация Мо заменяется на тетраэдрическую; в воль-фрамате координация W остается октаэдрической. [22]
Установлено, что рН среды оказывает большое влияние на характер полярограмм фталевой кислоты. В небуферных растворах бифталата калия появляются две волны. При добавлении катионов бария или кальция появляется еще третья волна. В буферных растворах при рН 3 6 получается одна волна. Добавление небольшого количества ионов бария понижает ее; при увеличении концентрации ионов бария появляется вторая волна. Фурман и Брикер76 предполагают, что вторая волна вызвана восстановлением комплекса, образовавшегося в результате взаимодействия ионов бария с бифта-латом. Высота первой волны в буферных растворах при рН2 6 - 4 1 в присутствии избытка бария пропорциональна концентрации недиссоциированной кислоты. [23]
В результате должен возникнуть градиент рН, так как перенос каждого одновалентного катиона должен сопровождаться освобождением одного протона во внешней среде. В работах [3, 53-55] действительно показано, что добавление проникающих синтетических катионов ДДА, ТФМФ, ТБА ( см. рис. 6.15) к митохондриям вызывает увеличение концентрации Н в среде. Изменения рН исчезают при добавке разобщителей. [24]
Еще более ярко взаимное усиление действия органических ионов проявляется при электровосстановлении аниона персульфата. Как видно из рис. 5.14, ингибирующий эффект аниона гексилсульфоната на разряд аниона SgOg2 - резко усиливается в присутствии катиона ТБА. Анализ адсорбционных данных в этой системе показывает, что усиление ингибирующего действия органического аниона при добавлении катиона ТБА связано с увеличением адсорбции органического аниона при его соадсорбции с катионами ТБА. Если совместно адсорбируются нейтральное ПАОВ, например цетиловый спирт, и катионы ТБА, то их ингибирующие действия на скорость восстановления НзО аддитивно складываются. При этом как при адсорбции отдельных добавок, так и при их соадсорбции природа медленной стадии реакции не изменяется. [25]
Для больших молекул типа конденсированных полициклических ароматических и гетероциклических соединений решающим является использование широкопористых катализаторов, что облегчает доступ их к активным местам. Однако при создании и применении материалов с очень большими порами механическая прочность катализаторов резко снижается. Недавнее исследование [32] показывает, что этот недостаток в случае оксида алюминия может быть до некоторой степени исправлен добавлением катионов щелочных и щелочно-земель-ных металлов. Не ясно, что приводит к улучшению механических свойств, - образование более жесткой кристаллической решетки или увеличение адгезии между частицами, которые образуют структуру оксида алюминия в таблетке катализатора. [26]
Качественный характер влияния малых добавок на скорость окисления металлов описывается теорией Вагнера. Мп и Fe полностью согласуется с положением Вагнера о том, что скорость окисления металлов, образующих полупроводниковые окислы с недостатком металла, повышается при добавлении катионов с более высокой валентностью. [27]
Добавим здесь несколько замечаний относительно величины рН в дождевой воде. На протяжении большей части года значения рН находились между 4 и 5 в южной части Швеции и вдоль берегов Балтики и Атлантики до северной части Норвегии. Факторы, которые определяют эту общую картину, довольно сложны. Низкие значения в южной части Швеции и частично вдоль побережья, вероятно, обусловлены загрязнением из Центральной и Западной Европы. Эта точка зрения подтверждается сезонными изменениями с наиболее низкими значениями зимой, когда воздушный поток направлен с юга и загрязнение имеет максимум. Поскольку SO2 - одна из важнейших составляющих загрязнения, вероятно, что серная кислота является регулирующим фактором для рН в этом районе. Однако низкие значения рН вдоль большей части побережья Норвегии и над Балтикой нельзя объяснить искусственным SO2, и они могут быть связаны с образованием H2S в естественных условиях в береговых участках или в море, как отмечалось для Западной Европы. Более высокие значения рН в глубине суши вызываются либо увеличивающимся выведением SO2, либо добавлением катионов, таких, как Са2 или NHr. [28]
Страницы: 1 2