Добавление - кислота
Cтраница 2
Добавление кислот и щелочей вызывает изменение рН дрожжевой суспензии, которое может привести к изменению зарядов как дрожжевых клеток, так и макромолекул продуктов метаболизма. [16]
Добавление кислоты к белому тесту сильно увеличивает эффект термической обработки. [17]
Добавление кислоты к белому тесту сильно повышает эффект термической обработки. Предполагают также, что действие кислоты связано с частичным разложением белого теста и гидролизом HCN с образованием групп NH4, заменяющих часть калия. [18]
Добавление кислоты или щелочи во многие солевые растворы приводит к значительно меньшему сдвигу рН по сравнению с величинами, приведенными в табл. 1 для чистой воды. Способность таких растворов противостоять изменению рН называется буферным действием. [19]
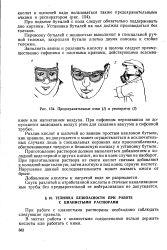 |
Предохранительные очки ( 1 и респиратор ( 2. [20] |
Добавление кислоты к нагретой воде не разрешается. [21]
Добавление кислоты к системе СаСО3 Са2 СО32 - также повышает растворимость осадка. [22]
Добавление кислот повышает антидетонационную стойкость только этилированных бензинов. С увеличением содержания ТЭС в бензинах эффективность действия кислот увеличивается и повышается оптимальная концентрация кислоты. Введение кислоты в высокооктановые бензины более эффективно, чем в низкооктановые. С повышением октанового числа бензина растет промотирующее действие кислот. [23]
 |
Распределение потерь ВАМВР в водные растворы Л. аС1 - aOlI, содержащие 0 9 ( /. 1 8 ( 2 и 3 1 М 1 ат ( 3. Соотношение Ув. F040. 1. Органическая фаза - i M ВАМВР в и-октаиг. [24] |
Добавление кислоты на последней ступени экстракции весьма эффективно предотвращает потери зкстрагента ( о-фенилфенол, 4-хлор - 2-феннлфснол) 119 ], по в случае ВАМВР оно излишне. [25]
Добавление кислот смещает равновесие реакции влево. [26]
Добавление кислоты в отработанную осадительную ванну необходимо не только для разложения сернистых соединений, но и для нейтрализации свободного аммиака, накапливающегося в ванне. [27]
Добавление кислоты и особенно щелочи вызывает смещение равновесия вправо и усиливает гидролиз. [28]
Добавление кислоты к воде приводит к увеличению [ Н ] и уменьшению [ ОН - ], а добавление щелочи - к обратному эффекту. Причем [ Н ] и [ ОН - ] меняются таким образом, что / Сн2о при данной температуре остается постоянной. Следовательно, концентрация ионов Н или ОН - может служить мерой кислотности или щелочности среды. [29]
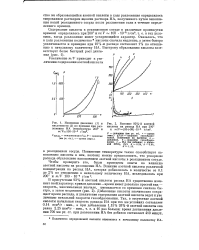 |
Изменение давления ( 1 и кислотности ( 2 по времени при разложении НА ( температура 200 и m / F 100 - 10 - 4 г / см3.| Влияние 93 % - и азотной. [30] |
Страницы: 1 2 3 4