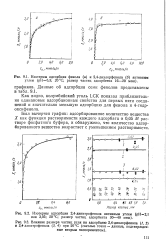
Адсорбированное количество - вещество
Cтраница 1
 |
Изотерма адсорбции где k - константа, зависящая от химической природы и. [1] |
Адсорбированное количество вещества следовало бы относить не к единице массы, а к единице поверхности, но для мелкораздробленных веществ и однородных суспензий ( например, взмученный животный уголь) эта поверхность растет пропорционально общей массе. [2]
Адсорбированное количество вещества может быть уменьшено или увеличено при сохранении постоянной температуры путем уменьшения или увеличения концентрации адсорбтива. [3]
 |
Изотерма адсорбции. [4] |
Адсорбированное количество вещества нужно было бы относить не к единице массы, а к единице поверхности, но для мелкораздробленных веществ и однородных суспензий ( например, взмученный животный уголь) эта поверхность растет пропорционально общей массе. [5]
Был вычерчен график: адсорбированное количество вещества X как функция растворимости каждого адсорбата в 0 05 М растворе фосфатного буфера, и обнаружено, что количество адсорбированного вещества возрастает с уменьшением растворимости. [7]
Выше было показано, что между изменением поверхностного натяжения, адсорбированным количеством вещества и температурой существует определенная связь, которая может быть выражена уравнением состояния адсорбционного слоя. Мы уже сидели, что адсорбированные молекулы в известных случаях можно рассматривать как газообразные, так как они способны перемещаться вдоль поверхности без затраты работы. [8]
Выше было показано, что между изменением поверхностного натяжения, адсорбированным количеством вещества и температурой существует определенная связь, которая может быть выражена уравнением состояния адсорбционного слоя. Мы уже видели, что адсорбированные молекулы в известных случаях можно рассматривать как газообразные, так как они способны перемещаться вдоль поверхности без затраты работы. [9]
Рассмотрим систему, состоящую из адсорбента любой геометрической структуры, содержащего предельно адсорбированное количество вещества as, и отдельно ( вне адсорбента) это же вещество в виде нормальной жидкости. Обе части системы сообщаются через газовую фазу. Вся система находится в замкнутом объеме при температуре плавления нормальной жидкости Тпл. В условиях равновесия давление пара адсорбата ра ртв равно давлению насыщенного пара жидкости. Так как температура для всей системы одна и та же, условием ее равновесия при любых температурах ниже T будет равенство давления пара адсорбата над адсорбентом и насыщенного пара этого же вещества в кристаллическом состоянии вне адсорбента. [10]
Рассмотрим систему, состоящую из адсорбента любой геометрической структуры, содержащего предельно адсорбированное количество вещества as, и отдельно ( вне адсорбента) это же вещество в виде нормальной жидкости. Обе части системы сообщаются через газовую фазу. Вся система находится в замкнутом объеме при температуре плавления нормальной жидкости Тпя. В условиях равновесия давление пара адсорбата ра ртв равно давлению насыщенного пара жидкости. Так как температура для всей системы одна и та же, условием ее равновесия при любых температурах ниже Гпл будет равенство давления пара адсорбата над адсорбентом и насыщенного пара этого же вещества в кристаллическом состоянии вне адсорбента. [11]
Для выяснения механизма адсорбции необходимо построить изотерму адсорбции, выражающую связь между адсорбированным количеством вещества и его равновесной концентрацией в растворе. [12]
Адсорбцию обычно характеризуют с помощью так называемой изотермы адсорбции, выражающей связь между адсорбированным количеством вещества Г и его равновесной ( при данных условиях) концентрацией в растворе. С целью определения изотерм адсорбции при постоянной температуре экспериментально изучают равновесное распределение адсорбата между адсорбентом и раствором. [13]
Следовательно, при адсорбции газов, паров или растворенных веществ реальными активными углями нельзя все адсорбированное количество вещества относить к объему микропор и находить по предельной адсорбции Wo истинные характеристики микропористой структуры адсорбентов. Очевидно, что из суммарной адсорбции необходимо вычесть адсорбцию на поверхности мезопор, и лишь остаточное количество адсорбированного вещества действительно заполняет микропоры. [14]
Ео многих случаях, вплоть до точки, в которой завершается построение первого слоя молекул, кривая зависимости адсорбированного количества вещества ( откладываемого по оси ординат) от давления ( ось; абсцисс) вогнута к оси абсцисс и сходна по своей форме с простой изотермой Лэнгмюра; правда, это не всегда имеет место: например, при адсорбции кислорода на хлористом калии кривая может иметь почти линейный ход. При дальнейшем повышении давления адсорбция сначала ( после построения первого слоя) растет медленнее, чем раньше, но по мере приближения к точке конденсации скорость ее роста с давлением повышается все больше и больше, достигая под конец огромного значения. В нескольких случаях наблюдались изломы кривой, которые можно связывать с завершением построения отдельных молекулярных слоев. Вообще же количество вещества, адсорбируемое после построения первого слоя, позволяет заключить, что объемная конденсация на этих плоских поверхностях начинается уже после адсорбции всего лишь 4 - 5 слоев. [15]
Страницы: 1 2