Добавление - концентрированный раствор
Cтраница 3
Хинолин и непрореагировавший анилин отгоняют с водяным паром, дистиллят экстрагируют эфиром ( 3 раза по 30 мл) и после отгонки эфира сырые основания растворяют в смеси 25 мл концентрированной НС1 и 100 мл воды. Соль разлагают добавлением концентрированного раствора NaOH до щелочной реакции по фенолфталеину и перегоняют вторично с водяным паром. Хинолин извлекают эфиром, эфирные вытяжки сушат над твердой щелочью. [31]
Выпавшую после охлаждения двойную соль хинолина отфильтровывают на воронке Бюхнера, тщательно отжимают и промывают на фильтре 12 мл 2 моль л НС1 для удаления анилина. Двойную соль разлагают добавлением концентрированного раствора щелочи до щелочной реакции по фенолфталеину и перегоняют выделившийся хинолин с водяным паром. [32]
В преддверии обсуждения шиммирования в разд. Если вы готовите образец добавлением концентрированного раствора вещества в ампулу с требующимся количеством растворителя, то его необходимо тщательно перемешать. Причиной удивительного и необъяснимого ухудшения разрешения может оказаться наличие неперемешавшихся слоев разной концентрации в ампуле диаметром 5 мм. Образование воронок в таких слоях очень сильно ухудшает разрешение, особенно в сильных полях. [33]
Таким сбразом, на положительно заряженные частицы коллоидов коагулирующее действие оказывают анионы, на отрицательно заряженные-катионы причем, чем выше заряд аниона или катиона, тем более сильное коагулирующее действие они оказывают. Некоторые коллоиды коагулируют при добавлении концентрированных растворов солей ( высаливание) или при добавлении другого растворителя. Повышение температуры раствора также способствует коагуляции. Коагуляция коллоидов имеет большое значение в анализе. С целью предотвращения образования коллоидов при осаждении гидроокисей и сульфидов катионов III аналитической группы сульфидом аммония к последнему добавляют хлорид аммония, способствующий коагуляции коллоидов. [34]
Таким образом, на положительно заряженные частицы золей коагулирующее действие оказывают анионы, на отрицательно заряженные - катионы, причем, чем выше заряд аниона или катиона, тем большее коагулирующее действие они оказывают на соответствующие золи. Некоторые золи коагулируют лишь при добавлении концентрированных растворов солей ( высаливание) или при добавлении другого растворителя. Повышение температуры раствора в ряде случаев способствует коагуляции. Гели, образуемые из золей в процессе их коагуляции, представляют собой дисперсные системы, отличающиеся развитой пространственной структурой ( сеткой) - каркасом. Пространственная сетка характеризуется различной степенью объемного заполнения системы частицами дисперсной фазы, обусловливаемого силами молекулярного сцепления. Коагуляция золей имеет большое значение в анализе. С целью предотвращения образования золей при осаждении гидроокисей и сульфидов катионов III аналитической группы сульфидом аммония к нему добавляют хлорид аммония, способствующий коагуляции. [35]
К 50 мл анализируемого раствора, содержащего 15 - 20 мг кобальта, прибавляют в избытке титрованный раствор ЭДТА, точно его отмеривая. Затем приводят рН раствора к 10 добавлением концентрированного раствора аммиака, прибавляют индикатор в количестве, достаточном для получения чисто голубой окраски, и титруют раствором соли цинка до перехода окраски в красную. [36]
Затем приводят рН раствора к 10 добавлением концентрированного раствора аммиака, прибавляют индикатор в количестве, достаточном для получения чисто голубой окраски, и титруют раствором соли цинка до перехода окраски в красную. [37]
К 5Q мл анализируемого раствора, содержащего 15 - 20 мг кобальта, прибавляют в избытке титрованный раствор ЭДТА, точно его отмеривая. Затем приводят рН раствора к 10 добавлением концентрированного раствора аммиака, прибавляют индикатор в количестве, достаточном для получения чисто голубой окраски, и титруют раствором соли цинка до перехода окраски в красную. [38]
Таким образом, на положительно заряженные частицы коллоидов оказывают влияние анионы, на отрицательно заряженные-катионы, причем высоковалентные анионы и катионы оказывают более сильное коагулирующее действие, чем одновалентные. Некоторые коллоиды коагулируют при высаливании ( добавлении концентрированных растворов солей) или при добавлении другого растворителя. Повышение температуры раствора также способствует коагуляции. [39]
Осмеат натрия Na2OsO4 образуется при введении твердой или газообразной четырехокиси в раствор едкого натра в присутствии слабого восстановителя ( например, спирта), раствор при этом окрашивается в темно-пурпуровый цвет. Калиевая соль красно-фиолетового цвета получается таким же путем или добавлением концентрированного раствора едкого кали к раствору осмеата натрия. [40]
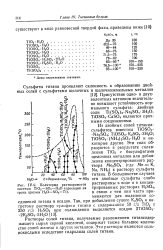 |
Политерма растворимости системы ТЮ2 - SO3 - H2O ( проекция на грань призмы Н2О - SO3 - Ti. [41] |
Из двойных солей титанил-сульфатов известны TiOSCV Na2SO4; TiOSO4 - K2SO4 - 3H2O; TiOSO4 - ( NH4) 2SO4 - H2O и некоторые другие. Эти соли образуются в результате сплавления ТЮ2 с бисульфатами щелочных металлов или добавления концентрированного раствора Me2SO4 ( где Me К, Na, NH4) к раствору сульфата титана. [42]
В частности, этот электрод позволяет проводить прямое определение азота в ионах аммония. При анализе мочевины уреаза катализирует разложение мочевины до NH - ионов, которые после добавления концентрированного раствора щелочи образуют свободный аммиак. Аммиак диффундирует через газопроницаемую мембрану к электроду, после чего устанавливается равновесие газ - жидкость с внутренним раствором электрода. Ионы гидроксила, образовавшиеся во внутреннем растворе при ионизации гидроксида аммония, смещают потенциал внутреннего электрода таким образом, что он оказывается пропорциональным содержанию аммиака в пробе. Равновесие устанавливается приблизительно за 1 мин, а электродный потенциал зависит от концентрации аммиака в пробе точно по уравнению Нернста. [43]
Обычно гидробромиды и гидроиодиды менее растворимы в воде, чем гидрохлориды, и могут быть получены добавлением концентрированного раствора бромистого или йодистого калия к раствору соответствующего гидрохлорида. Перхлораты, нитраты и оксалаты некоторых органических оснований обладают умеренной растворимостью. [44]
Ангидрооксимеркури-соединение почти не растворимо в воде и в большинстве органических растворителей, легко растворяется оно лишь в щелочах. Из слабощелочного раствора может быть выделена натриевая соль в виде красивых серебристых иголок, высаливанием при помощи поваренной соли или добавлением концентрированного раствора едкого натра. [45]
Страницы: 1 2 3 4