Дальнейшее добавление - щелочь
Cтраница 1
Дальнейшее добавление щелочи при рН9 - 10 разрушает комплекс; при этом галлий остается в растворе, по-видимому, в виде галлата. [1]
 |
Состав раствора малеиновой кислоты ( Н2М в зависимости от рН. [2] |
При дальнейшем добавлении щелочи доля НМ - убывает, а доля М2 - растет. [3]
 |
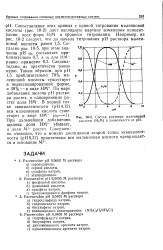
Кривая титрования сильной кислоты сильным основанием. [4] |
При дальнейшем добавлении щелочи - свыше 100 % - рН продолжает повышаться. [5]
При дальнейшем добавлении щелочи в растворе появляются ионы гидроксила и электропроводность снова возрастает. Таким образом, в точке нейтрализации система обладает минимумом электропроводности. Кондуктометрическое титрование применяется и при реакциях, сопровождающихся образованием осадков. В зависимости от природы исходных веществ и продуктов реакции осаждения в точке эквивалентности наблюдают или минимум электропроводности, или резкое ее возрастание. Во втором случае до точки эквивалентности электропроводность остается практически постоянной. [6]
 |
Ход кривой титрования при [ IMAGE ] Схема установки для опре. [7] |
По достижении рН гидроксидообразования дальнейшее добавление щелочи в раствор не приводит к повышению величины рН до тех пор, пока не завершится процесс образования гидроокиси. [8]
 |
Схема прибора для кондуктометрического титрования. [9] |
По достижении точки конца титрования дальнейшее добавление щелочи приводит к накоплению в растворе гидроксид-ионов. Поскольку молярная электрическая проводимость ионов водорода наибольшая по сравнению с другими ионами, то графическая зависимость электрической проводимости от объема добавляемой щелочи имеет своеобразный вид, приведенный на рис. 12.12, а прибор, используемый для проведения кондуктометрического титрования, показан на рис. 12.13 ( о потенциометрическом титровании см. в разд. [10]
Обратите внимание, что в первой пробирке образовавшийся вначале осадок гидроксида хрома при дальнейшем добавлении щелочи растворяется, а при нагревании снова выпадает в виде серо-зеленой массы. Во второй пробирке выпавший осадок гидроксида алюминия растворяется в избытке гидроксида натрия, но при нагревании осадка не образуется. [11]
Обратите внимание, что в первой пробирке образовавшийся вначале осадок гидроокиси хрома при дальнейшем добавлении щелочи растворяется, а при нагревании снова выпадает в виде серо-зеленой массы. Во второй пробирке выпавший осадок гидроокиси алюминия растворяется в избытке щелочи, но при нагревании осадка не образуется. [12]
В области 1350 см-1 в спектрах ком - ОПДТУ f Fe C13; 5 - плексов Fe и Ег имеются полосы в виде Nas ОПДТУ плеча, исчезающие при дальнейшем добавлении щелочи. Подобные полосы отсутствуют в спектрах комплексов Си, Zn и соли Na5 ОПДТУ. [13]
Было бы интересно выяснить, не будет ли добавление нейтрального мыла в дополнение к небольшим количествам щелочи, обусловливающим максимумы, вызывать такое же падение поверхностного натяжения, как и дальнейшее добавление щелочи. [14]
Вскоре после прибавления первых порций сильного основания рН раствора станет равным 3 1 и раствор окрасится в оранжевый цвет, а при рН4 4 раствор окрасится в желтый цвет, не изменяющийся при дальнейшем добавлении щелочи. [15]
Страницы: 1 2 3