Комплекс - индикатор
Cтраница 2
Металлиндикаторы - это обычно красители, образующие с ионами металлов комплексы, окраска которых отличается от окраски не связанного в комплекс индикатора. Поскольку ме-таллиндикаторы являются обычно и индикаторами на ион водорода, то для каждого индикатора характерны особые условия как кислотно-основного равновесия, так и равновесия с ионами металла. [16]
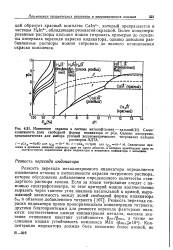
Сплошными прямыми и кривыми линиями отделены друг от друга области, в которых преобладает одна из соответственно окрашенных форм индикатора и комплекса индикатора с кальцием. [18]
Титрование с эриохромом черным Т проводят при рН 8 - 9 в кипящем растворе, содержащем тартрат-ионы; рН раствора не должен быть выше 9, так как иначе комплексы индикатора с металлами оказываются настолько прочными, что не разрушаются под действием ЭДТА. Прибавление тартрат-ионов необходимо для предотвращения выпадения гидроокисей металлов, а кипячение ускоряет реакцию. Основываясь на аналогии в химическом поведении и на сравнительной близости значений констант устойчивости комплексов редкоземельных металлов, можно предсказать, что и другие представители этой группы металлов будут вести себя аналогично. Действительно, практически все трехвалентные ионы редкоземельных металлов, за исключением прометия, можно титровать комплексонометрически. Определениям мешает CeIV, но его можно легко восстановить аскорбиновой кислотой. [19]
Одним из часто применяемых индикаторов на ион кальция является мурексид. Раствор этого индикатора при рН 10 имеет синюю окраску, а комплекс индикатора с кальцием - красного цвета. [20]
Фта-леиновый пурпуровый, рекомендуемый Белчером и др. [ 58 ( 2) ], также может служить индикатором в аммиачном растворе, однако он блокируется ионами многих металлов, в том числе и цинка. На основании своих исследований, которые позволили разработать метод последовательного титрования смеси цинка с кадмием, использовав вышеупомянутый принцип, Флашка полагает, что, по-видимому, образуется комплекс индикатора с цинком, который настолько сильно диссоциирует, что индикатор подвергается окислительному или гидролитическому разложению. В более прочном комплексе с кадмием индикатор делается стабильным. [21]
В комплексонометрии применяют индикаторы, дающие окрашенное соединение с определяемым ионом. Примером такого индикатора служит эриохром черный Т ( кислотный хром черный специальный), который с ионами магния, кальция и некоторыми другими образует комплексы, интенсивно окрашенные в винно-красный цвет. Раствор не связанного в комплекс индикатора окрашен в синий цвет. Переход окраски от винно-красной к синей отчетлив, поэтому эриохром черный Т является чувствительным индикатором. [22]
При рН ниже 6 в растворе находятся однозарядные анионы красного цвета, при рН 7 - 11 - двухзарядные анионы синего цвета, а при рН выше 12 - трехзарядные анионы желто-оранжевого цвета. Комплекс кобальта с эриохромчерным Т, образующийся при рН около 10, имеет красный цвет. В точке эквивалентности происходит переход синей окраски ( цвет свободного красителя) в красную ( цвет комплекса индикатора с ионами цинка и др.); необходимое рН раствора, равное 10, устанавливают аммиачным буферным раствором. [23]
 |
Наиболее распространенные оксред-индикаторы. [24] |
Металлоиндикаторы ( металлохромные индикаторы) используют в комплексометрическом титровании. Это красители, которые образуют с ионами металлов ( М) окрашенные комплексы Mind, менее стойкие, чем комплекс того же металла с ЭДТА. Краситель и его комплекс различаются по окраске. Изменение окраски происходит в тот момент, когда при титровании ЭДТА комплекс индикатора с металлом полностью разрушается, замещаясь более прочным комплексом металла с титрантом, и раствор приобретает окраску свободного индикатора. [25]
Для питьевых, подземных и поверхностных вод согласно ГОСТ 4151 - 72 определяется общая жесткость. Это определение проводится комплексонометрическим методом. Он основан на связывании ионов кальция и магния в комплексные соединения, сопровождающемся изменением окраски индикатора. Чувствительность этого метода зависит от чувствительности применяемых индикаторов и составляет 1 - 2 мкг-экв / л ( для индикаторов кислотный хром синий марки К и кислотный хром темно-синий), при меньшей жесткости окраска комплексов индикаторов с ионами кальция и магния уже не отмечается визуально. [26]
Для питьевых, подземных и поверхностных вод согласно ГОСТ 4151 - 72 определяется общая жесткость. Это определение проводится комплексонометрическим методом. Он основан на связывании ионов кальция и магния в комплексные соединения, сопровождающемся изменением окраски индикатора. Чувствительность этого метода зависит от чувствительности применяемых индикаторов и составляет 1 - 2 мкг-экв / л ( для индикаторов кислотный хром синий марки К и кислотный хром темно-синий), при меньшей жесткости окраска комплексов индикаторов с ионами кальция и магния уже не отмечается визуально. [27]
Страницы: 1 2