Комплекс - ион - переходный металл
Cтраница 1
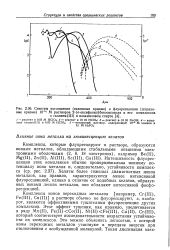 |
Спектры поглощения ( сплошные кривые и флуоресценции ( штриховые кривые 10 - 4 М растворов 2 - ( о-оксифенил бензоксазола и его комплексов с галлием ( III в изоамиловом спирте. [1] |
Комплексы ионов переходных металлов [ например, Сг ( П1), Fe ( III), Cu ( II) ] в растворе обычно не флуоресцируют, а, наоборот, являются эффективными тушителями флуоресценции других комплексов. Этот эффект тушения, как правило, увеличивается в ряду Mn ( II), Fe ( II) Co ( II), Ni ( II) Fe ( III), Cu ( II), Cr ( III), который соответствует последовательности возрастания устойчивости их комплексов. Это можно объяснить легкостью, с которой ионы переходных металлов участвуют в передаче энергии при столкновении с возбужденной молекулой. [2]
Комплексы ионов переходных металлов имеют незаполненные d - орбитали. Энергия, требуемая для возбуждения электрона в таких комплексах с орбитали / 2g на eg, часто соответствует длинам волн света в видимой области. Следовательно, поглощение света может вызывать указанные электронные переходы. [3]
 |
Система координат ( нештрихованная для шестикоординационного комплекса ( А, локальная ( штрихованная система координат ( Б, определение 9 и ср, данных в ( В. [4] |
В комплексах ионов переходных металлов картина значительно усложняется, поскольку мы имеем дело с перекрыванием с / - орбиталей и располагаем многими лигандами. Система координат, показаннная на рис. 10.25 Л, фиксирует положение истинных d - орбиталей этого комплекса. [5]
В комплексах ионов переходных металлов член S-D-S используют для описания любого эффекта, который снимает спиновое вырождение, включая дипольные взаимодействия и спин-орбитальное расщепление. Низкосимметричное кристаллическое поле часто приводит к большим эффектам нулевого поля. [6]
Величина IQDq для комплексов ионов переходных металлов, принадлежащих к разным периодам периодической системы, но имеющих одинаковую электронную оболочку, примерно постоянна при однотипном лигандном окружении. [7]
Величина lODq для комплексов ионов переходных металлов, принадлежащих к разным периодам периодической системы, но имеющих одинаковую электронную оболочку, примерно постоянна при однотипном лигандном окружении. [8]
Величина IQDq для комплексов ионов переходных металлов, принадлежащих к разным периодам периодической системы, но имеющих одинаковую электронную оболочку, примерно постоянна при однотипном лигандном окружении. [9]
Некоторые комплексы, например комплексы ионов переходных металлов с этилендиаминтетраацетат-ионом и его производными, настолько устойчивы, что n N даже при наивысших исследованных кислотностях раствора; в таких системах константы устойчивости нельзя рассчитать из измерений концентрации свободных ионов водорода. Методы изучения наиболее устойчивых комплексов 1: 1 обсуждаются в разд. [10]
В конденсированной фазе у комплексов ионов переходных металлов первого ряда значения g - фактора не только не отвечают этому выражению, но часто отклоняются также от чисто спиновых значений. [11]
При исследовании методом ЭПР монокристаллов комплекса ионов переходных металлов обычно обнаруживают [13-15] комплексы, в которых в очевидной системе координат кристаллического поля д - и А-тензоры не диагональны. Ось, которая перпендикулярна зеркальной плоскости или совпадает с осью вращения, должна быть одной из трех главных осей молекулы. Тензор молекулы и Л - тензор для любого атома, лежащего на этой оси, должны иметь главные значения вдоль этой координаты. Если в молекуле есть только одна ось, которая удовлетворяет приведенным выше требованиям, две другие оси, используемые в качестве базиса при анализе в кристаллическом поле, не обязательно будут главными осями соответствующих д - и А-тензоров, т.е. выбор этих осей не обязательно приведет к диагональному тензору. Ось вращения второго порядка является одной из осей, приводящих соответствующие компоненты д - и / 1-тензоров к диагональному виду, но две другие компоненты не диагональны в системе координат, соответствующей осям кристаллического поля. Если молекула обладает симметрией D2h, то три оси вращения второго порядка этой точечной группы должны быть главными осями как для g - тензора, так и для Л - тензора. Таким образом, результаты исследования методом ЭПР могут дать информацию относительно симметрии молекулы. Для несимметричной молекулы совсем не обязательно, чтобы молекулярные оси совпадали с осями, которые приводят g - тензор или Х - тензор к диагональному виду. На самом деле система координат, приводящая Л - тензор к диагональному виду, может и не диагонализировать g - тензор. [12]
Как мы увидим в главах, посвященных ЭПР и ЯМР комплексов ионов переходных металлов, эти данные применяются в нескольких важных областях. Анизотропию магнитной восприимчивости обычно определяют методом Кришнана, устанавливая критический момент вращения. В статье [31] рассматривается использование метода ЯМР для измерения магнитной восприимчивости веществ в растворе. Раствор парамагнитного комплекса, содержащий внутренний стандарт, вводят в объем между двумя концентрическими трубками. Раствор того же самого инертного стандарта в том же самом растворителе, в котором растворен комплекс, вводят во внешнюю часть конструкции. В этом случае наблюдаются две линии стандарта, причем линия вещества, введенного в раствор парамагнитного комплекса, соответствует более высокой частоте. [13]
Знак и величина градиента поля могут быть использованы для получения информации об электронном основном состоянии комплекса иона переходного металла. [14]
В связи с усиленным ростом промышленного производства синтетических полимерных материалов методы инициирования радикальных реакций полимеризации с помощью комплексов ионов переходных металлов приобретают все большее значение. [15]
Страницы: 1 2