Комплекс - кальций
Cтраница 2
В заключение следует еще привести интересный метод определения констант устойчивости комплексов кальция и стронция основанный на биологических свойствах. [16]
 |
Кривые спектрофотометрического комплексометрического титрования кальция в присутствии мурексида ( а и меди ( II в аммиачной среде ( б. [17] |
В точке эквивалентности, когда комплекс кальция с мурексидом разрушается и образуется комплекс кальция с ЭДТА, наблюдается резкое уменьшение светопоглощения. За точкой эквивалентности поглощение снова остается постоянным. Титрант вблизи точки эквивалентности следует добавлять небольшими порциями, чтобы точно зафиксировать резкое изменение светопоглощения. [18]
Титруют при рН 12 5, в эквивалентной точке исчезает желто-зеленая флуоресценция, вызываемая комплексом кальция с флуорексоном и появляется розовая окраска свободного индикатора. [19]
Для определения содержания кальция в йодистом натрии кальций необходимо экстрагировать из анализируемого раствора, поскольку иод гасит флуоресценцию комплекса кальция с реагентом. [20]
Магний и кальций образуют устойчивые комплексы с ЭДТА при рН 10, в то же время при рН 7 6 устойчив только комплекс кальция. [21]
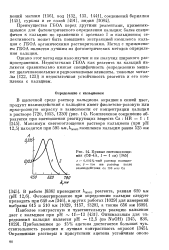 |
Кривые светопоглощения ( СФ-4А, 1 I см. [22] |
Преимущества ГБОА перед другими реагентами, применяющимися для фотометрического определения кальция: более специфичен к кальцию по сравнению с арсеназо I и кальционом; селективность может быть повышена экстракцией комплекса кальция с ГБОА органическими растворителями. Метод с применением ГБОА является лучшим из фотометрических методов определения кальция. [23]
Так, если для производных щавелевой кислоты, а-аланина, аспарагиновой кислоты, глицина, глютаминовой кислоты и некоторых других лигандов мы имеем нормальный ряд по устойчивости ( Mg Са Sr Ва), то для комплексонов обычным является максимум устойчивости у комплексов кальция. Возможно, это связано с тем, что соответствующие лиганды по отношению к ионам большего объема проявляют более высокие значения координационной емкости. [24]
Так, если для производных щавелевой кислоты, сс-аланина, аспарагиновой кислоты, глицина, глютаминовой кислоты и некоторых других лигандов мы имеем нормальный ряд по устойчивости ( Mg [ Са Sr Ba), то для комплексонов обычным является максимум устойчивости у комплексов кальция. Возможно, это связано с тем, что соответствующие лиганды по отношению к ионам большего объема проявляют более высокие значения координационной емкости. [25]
Представляет интерес свойство триполифосфата ( для метафос-фата оно еде не исследовалось или исследовалось только на охлаждающих рассол ах97 - 98), заключающееся в торможении осаждения углекислого кальция или в способности образовывать вместо кристаллов с острыми гранями, повреждающими волокно, хлопьевидные осадки СаСО3 или триполифосфатных комплексов кальция. [26]
Трилоном Б титруют ионы кальция, предварительно связанные с индикатором - мурексидом. Комплекс кальция с трилоном Б более прочен, чем комплекс с мурексидом. [27]
Обычно вместо указанного автором индикатора применяют более доступный индикатор-мурексид. Поскольку комплекс кальция с мурек-сидом относительнб малоустойчив, переход окраски в конце титрования не очень резкий. Для улучшения его была предложена смесь: 10 г хлорида натрия, 0 2 г мурексида, 0 5 г нафтолового зеленого В. Этой смеси добавляют 40 мг. [28]
Обычно вместо указанного автором индикатора применяют более доступный индикатор-мурексид. Поскольку комплекс кальция с мурек-сидом относительно малоустойчив, переход окраски в конце титрования не очень резкий. Для улучшения его была предложена смесь: 10 г хлорида натрия, 0 2 г мурексида, 0 5 г нафтолового зеленого В. Этой смеси добавляют 40 мг. [29]
Барий и стронций дают аналогичную реакцию, однако небольшие количества их могут быть связаны углекислым натрием. В этом случае комплекс кальция с реактивом экстрагируют хлороформом. [30]
Страницы: 1 2 3 4