Комплекс - трехвалентный кобальт
Cтраница 1
Комплексы трехвалентного кобальта, как правило, диамаг-итны. [1]
Комплексы трехвалентного кобальта получают окислением: Со2 в растворах в присутствии соответствующих лигандов. [2]
Подобно комплексам трехвалентного хрома комплексы трехвалентного кобальта достаточно устойчивы. Несмотря на то, что свойства соответствующих комплексов трехвалентных хрома и кобальта очень близки, стандартные методы, используемые для их получения, часто сильно различаются. Обычно комплексы трехвалентного кобальта получаются с большей легкостью, при этом используется метод окисления подходящего комплекса двухвалентного кобальта. Во всех случаях образуется диамагнитный комплекс трехвалентного кобальта. Превращение двухвалентного кобальта в трехвалентный происходит самопроизвольно с большой легкостью за счет кислорода воздуха. Чтобы предотвратить этот процесс, рекомендовано использовать различные окислители. [3]
Известен вариант титрования [1203] комплекса трехвалентного кобальта с комплексоном III раствором соли двухвалентного хрома. [4]
Вследствие более высокой устойчивости комплексов трехвалентного кобальта по сравнению с двухвалентным окисление соединений последнего идет даже под действием кислорода воздуха. [5]
Фотометрические методы определения кобальта в форме окрашенных аммиачных, бикарбонатных, оксалатных, сульфо-салицилатных комплексов трехвалентного кобальта, гексанит-рокобальтиата натрия и др. на практике применяются сравнительно редко. [6]
 |
Некоторые реакции комплексов рутения с третичными фосфинами. Следует отметить, что разные фосфины могут давать разные продукты. [7] |
Существует много диамагнитных кинетически устойчивых октаэд-рических комплексов, сходных с комплексами трехвалентного кобальта. Отличия от комплексов кобальта ( III) состоят в следующем. Во-вторых, не удается, за исключением особых обстоятельств для родия, восстановить трехвалентные комплексы до двухвалентных. [8]
В этой же таблице приведены также некоторые устойчивые к сильному подкнслепию комплексы трехвалентного кобальта и хрома. Для этих комплексов состояние с сильно проявленной внутримолекулярной ионизацией устойчиво в течение продолжительного времени. [9]
При окислении бромом на холоду [49] комплекса с двухвалентным кобальтом образуются комплексы трехвалентного кобальта, в которые этилендиаминтетрауксусная кислота входит только в виде пятизубчатого адденда, а шестое место в координационной сфере металла занимает ион брома. Анион CoYBr2 - окрашен в темно-зеленый цвет. Шварценбах выделил следующие его соли: LiHCoYBr 4Н2О, NaHCoYBr 2Н2О ( аналогичный состав имеют калиевые, рубидиевые, цезиевые и аммонийные соли), Mg [ Co ( HY) Вг ] 2 12Н20, Co [ Co ( HY) Br ] 2 10Н20, Ba [ Co ( HY) Br ] 2 5Н20, N ( CH3) 4Co ( HY) Br ] 4Н2О и дигидрат аналогичной соли пиперидина. Эти соли относительно нестойки и легко, особенно при нагревании, отщепляют ион брома. Эти комплексные соединения более устойчивы, чем аналогичные комплексы с ионом брома в качестве второго адденда. [10]
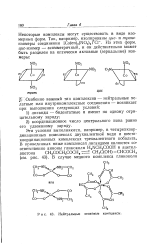 |
Нейтральные хелатные комплексы. [11] |
Эти условия выполняются, например, в четырехкоор-динационных комплексах двухвалентной меди и шести-координационных комплексах трехвалентного кобальта. [12]
Аналогичный комплекс трехвалентного марганца MnY нестоек и разрушается даже при слабом нагревании. Таким способом получается смесь связанных в комплекс трехвалентного кобальта и двухвалентного марганца. [13]
Цистеин HS - CH2 - CH ( NH2) COOH дает с солями кобальта при рН 7 - 8 в отсутствие окислителей комплексное соединение двухвалентного кобальта, окрашенное в оливково-зеленый цвет. Этот комплекс быстро окисляется воздухом или в присутствии окислителей, образуя комплекс трехвалентного кобальта H3Co ( SCH2NH2CHCOO) 3, окрашенный в коричневый цвет. Никель при тех же условиях дает комплексное соединение бордово-красного цвета. [14]
О, никогда не входит в такие комплексы. В-третьих, неизвестно, почему переходные металлы образуют так много координационных соединений, а некоторые другие металлы - так мало и почему, в частности, комплексы трехвалентного кобальта ( и в меньшей степени хрома) обладают такой замечательной устойчивостью сравнительно, например, с соединениями трехвалентного железа. Аналогичные соединения трехвалентного никеля в действительности неизвестны. Очевидно, нужно найти способ изучения групповых свойств структур, состоящих из восьми или двенадцати общих электронов, для того чтобы установить причину устойчивости данной конфигурации в определенных атомах и вычислить прочность и расположение этих связей. Кроме того, как мы нашли раньше, недостаточно учесть только внешнюю электронную структуру атома, одинаковую, например, у кислорода и серы. [15]
Страницы: 1 2