Комплекс - олово
Cтраница 1
Комплексы олова, тантала, ниобия, германия и вольфрама нерастворимы в разбавленной серной кислоте, в то время как комплекс титана растворим. Комплексы олова, тантала, титана, ниобия и германия нерастворимы в слабокислых оксалатных растворах, полунасыщенных хлористым аммонием. Комплекс вольфрама является единственным комплексом, не осаждающимся из растворов, содержащих органические кислоты; но частичное его осаждение индуцируется другими элементами группы А. [1]
Осадок комплекса олова хорошо коагулирует, и дополнительной установки кислотности после добавления таннина не требуется. [2]
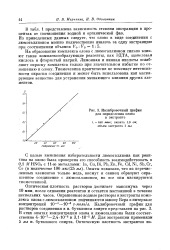 |
Калибровочный график. [3] |
На образование комплекса олова с люмогаллионом сильно влияют такие комплексообразующие реагенты, как ЭДТА, щавелевая кислота и фтористый натрий. Лимонная и винная кислоты ослабляют окраску комплекса только при значительном избытке по отношению к олову. Тиомочевина практически не изменяет интенсивности окраски соединения и может быть использована как маскирующее вещество для устранения мешающего влияния других элементов. [4]
Он состоит из экстракции комплекса олова с окисью т / шс - ( 2-этилгексил) - фосфина раствором циклогексана. [5]
В настоящей работе рассмотрены свойства комплекса олова с с люмогаллионом и условия экстракционно-фотометрического определения олова в индии без отделения основного вещества. [6]
Ионы рубидия и цезия осаждаются растворами галогенид-ных комплексов олова ( IV) в виде соединений Me2SnX6, где Me Rb или Cs, а Х С1, Вг, I. Эти комплексы применяются для отделения рубидия и цезия от калия. [7]
Как показали измерения, дипольные моменты комплексов четырех-хлористого олова и четыреххлористого титана с органическими сульфидами на 3 - 5Z) превышают сумму моментов компонентов, входящих в комплекс. Это свидетельствует о том, что межмолекулярная связь в этих соединениях носит донорно-акцепторный характер. [8]
 |
Стереохимия Sn ( IV. а - циклическая молекула [ 5п ( СбН5 21б ( фе. [9] |
Тетраздрическая система связен присутствует также в комплексах олова, содержащих фрагменты тина лиганд - SnCl3, например в ( C8Hi2) 3Pt3 ( SnCl3) 2 ( разд. [10]
Раствор имеет желтый цвет, а псевдораствор комплекса олова с фенилфлуороном - оранжево-красный. [11]
 |
Кривые зависимости значений потенциалов выделения висмута и меди из раствора тартрата от величины рН раствора. [ По J. J. L i п - g a n e, S. L. Jones, Anal. Chem., 23, 1798 ( 1951 ]. [12] |
Затем раствор делают очень кислым, чтобы разрушить комплекс олова ( IV) с тартрат-ионами, и осаждают олово. [13]
Затем раствор делают очень кислым, чтобы разрушить комплекс олова ( IV) с тартрат-ионами, и осаждают олово. [14]
Альтернативное объяснение состоит в предположении образования в реакции комплекса пентакоорди-национного олова, в котором происходит псевдовращение. Ранее возможность такой координации с участием растворителя была рассмотрена Насельским [24], который считает, что склонность R3SnHal к ассоциации приводит к стереохимической нежесткости. [15]
Страницы: 1 2