Комплекс - олово
Cтраница 2
Для фототурбидиметрического определения олова ( до 10 - 4 %) в ренийсодержащих материалах рекомендован комплекс олова ( 1У) с 9-феиил - 2 3 7-триокси - 6-флуороном. Введение в анализируемый раствор лимонной кислоты повышает избирательность метода и сокращает время образования окрашенного соединения до 3 мин. [16]
По той же причине увеличение содержания избытка едкого натра в электролите, сопровождающееся увеличением прочности щелочного комплекса олова, обусловливает уменьшение содержания олова в катодном осадке ( фиг. Изменение содержания избытка едкого натра в этом случае не влияет заметно на прочность медноцианистого комплекса. [17]
Аквакатион олова ( П) проявляет сильные кислотные свойства и поэтому устойчив только при рН 1 в среде хлорной или азотной кислот, анионы которых не обладают заметной склонностью входить в состав комплексов олова ( П) в качестве лигандов. При разбавлении таких растворов выпадают осадки основных солей различного состава. Большинство солей свинца ( П) ( например, иодид, хлорид, сульфат, хромат, карбонат, сульфид) малорастворимы в воде. [18]
Комплексы олова, тантала, ниобия, германия и вольфрама нерастворимы в разбавленной серной кислоте, в то время как комплекс титана растворим. Комплексы олова, тантала, титана, ниобия и германия нерастворимы в слабокислых оксалатных растворах, полунасыщенных хлористым аммонием. Комплекс вольфрама является единственным комплексом, не осаждающимся из растворов, содержащих органические кислоты; но частичное его осаждение индуцируется другими элементами группы А. [19]
Методика была проверена на образце металлического индия с известным содержанием олова ( 4 - 10 - 4 %), а также на образцах очищенной окиси индия с добавками. Соль индия была очищена экстракцией комплекса олова с люмогаллионом с последующим осаждением индия в виде гидроокиси и прокаливанием. [20]
Двухвалентное олово может присутствовать в растворе лишь в незначительных количествах ( до 0 5 мг), однако его влияние можно устранить введением в раствор винной кислоты. Следует отметить, что образование комплекса олова с винной кислотой протекает во времени; нагревание ускоряет зтот процесс. Поэтому титрование следует производить после предварительного подогрева раствора или примерно через 2 часа после приготовления. В этом случае присутствие даже 5 мг олова не отражается на результатах титрования. Титрование возможно и в присутствии небольших количеств галлия и никеля. Медь также мешает, однако ее влияние можно до некоторой степени устранить введением в раствор тиомочевины. В этом случае титрование возможно в присутствии до 0 5 мг меди. В таких же количествах допустимо и содержание свинца. Определение возможно при наличии в растворе до 2 мг мышьяка. Большие количества этих элементов затрудняют установление точки эквивалентности вследствие того, что медь, свинец и мышьяк дают диффузионный ток. Следует отметить, что присутствие мышьяка, меди и свинца в анализируемых продуктах не должно вызывать затруднений, так как эти элементы легко могут быть отделены от индия в ходе анализа: мышьяк и свинец - при разложении смесью соляной и серной кислот и упаривании раствора до появления паров серной кислоты, медь - при осаждении гидроокисей избытком аммиака. [21]
Мышьяк и сурьму можно также отделить от германия добавлением к раствору 10 г щавелевой кислоты, причем германий лереходит в гер-манооксалат, затем насыщают раствор сероводородом для осаждения мышьяка и сурьмы. Оксалатный комплекс германия, подобно комплексу олова, с сероводородом не реагирует. [22]
Направление, в котором сдвигается Ei / a с ростом концентрации фторида в этом случае, зависит от отношения р3 и р6, а также от координационных чисел. Фторидный комплекс олова ( IV) более стабилен, чем комплекс олова ( II), да и координационное число его больше. Поэтому при увеличении концентрации фторида наблюдается сдвиг Ei / z в катодном направлении в соответствии с обычными соотношениями свободных энергий. [23]
Лакост, Ирвинг и Уиберли [23] исследовали условия фотометрического определения различных металлов диэтилднтпокар-баматов натрия. Ими установлено, что комплексы олова и молибдена нестойки. Большая часть этих комплексов экстрагируется хлороформом в широких пределах рН, и в оптимальных условиях они подчиняются закону Бера при данных длинах волн, соответствующих максимальному светопоглощению. [24]
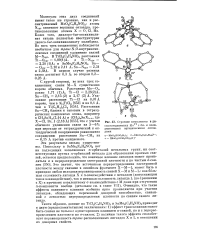 |
Строение комплексов в ди-оксосоединениях Мо с би - и поли-дентатными органическими лиган-дами. [25] |
Расстояние Мо-Ок равно 1 71 ( 1) А, Ti-Cl 2 28 ( 2) A, Sn - CH3 2 15 ( 2) и 2 17 ( 2) А. Расстояния Sn - СН3 близки к таковым в тетраэд-рических комплексах олова, например в GH3SnH3 ( 2 14 А) и ( СН3) 8пХ4 - п, где ХС1, Вг, J ( 2 18 А) 1655 ], что с учетом обычного удлинения связи на 5 - 6 % при переходе от тетраэдрической к ок-таэдрической координации равнозначно сокращению расстояния Sn - CH3 на - 0 15 А против ожидаемого. [26]
Элементы начала и конца больших периодов дают малопрочные роданидные комплексы, причем прочность слабо зависит от индивидуальности элемента. Направление изменений в ряде изученных случаев противоположно тому, которое наблюдается для элементов середины больших периодов. Так хлоридные и роданидные комплексы олова и сурьмы более прочны, чем соответствующие комплексы свинца и висмута. Следует отметить, что фторид-ные комплексы олова и сурьмы более прочны, чем комплексы свинца и висмута; для элементов середины больших периодов наблюдается обратная зависимость. [27]
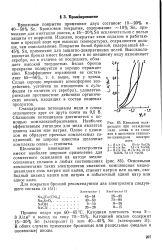 |
Катодная поляризация при осаждении меди, олова и их сплавов в щелочном станнат-но-цианидном электролите. [28] |
Стандартные потенциалы меди и олова отличаются друг от друга почти на 0 5 В. Сближение потенциалов достигается с помощью комплексообразования. Наиболее эффективным лигандом для меди является цианид калия или натрия. Олово с цианидом не образует прочных комплексных соединений, но широко известны щелочные комплексы олова - станнаты. [29]
Этот метод называют методом растирания порошков. Сухую пробу растирают с сухим реактивом. Метод был предложен в 1898 г. Ф. М. Флавицким, в некоторых случаях его применяют и в настоящее время, особенно часто его используют геологи в полевых условиях. Так, при растирании с диметилглиоксимом минерала, содержащего олово, образуется соединение фиолетового цвета. По-видимому, в этом случае образуется разноме-талльный комплекс олова, диметилглиоксима и железа, которое обычно также содержится в минералах и горных породах. [30]
Страницы: 1 2