Комплекс - первый тип
Cтраница 2
Для описания комплексов первого типа используются следующие эквива-лентные термины: низкоспиновые, спин-спаренные, комплексы сильного поля или внутреннеорбитальные, а для комплексов другого типа - термины: высокоспиновые, спин-свободные, комплексы слабого поля или внешнеорбитальные. [16]
 |
Константы устойчивости хелатных комплексов типа 1. 1 ионов Ln3 и Y3 ( для сравнения с полиаминполикарбоксилат-ионами ( imda2 - - имино. [17] |
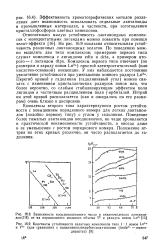
На рис. 16.9 показана относительная устойчивость различных лантаноидных хелатов. По поведению можно выделить два типа комплексов; примерами первого типа служат комплексы с лигандами edta и dcta, а примером второго-с лигандом dtpa. Комплексы первого типа отвечают ( по размерам и заряду ионов Ln3) простой электростатической ( или кислотно-основной) концепции. Перегиб кривой у гадолиния ( гадолиниевый угол) можно связать с изменением кристаллических радиусов ионов или, что более вероятно, со слабым стабилизирующим эффектом поля лигандов и частичным расщеплением поля f - орбиталей. Иттрий на этой кривой располагается ( как и ожидалось по его размерам) очень близко к диспрозию. [18]
Комплексы окисного железа распадаются на два основных класса. Некоторые комплексы, как Fe ( H2O) и FeFI, обладают высокими парамагнитными моментами, указывающими на наличие пяти неспаренных электронов; другие комплексы, как, например, Fe ( CN) e -, имеют гораздо меньшие моменты, соответствующие одному неспаренному электрону. Полинг первоначально предположил, что комплексы первого типа являются в основном ионными с пятью З - орбитами иона Fe3, занятыми неспаренными электронами по одному на каждой орбите, и с ли-гандами, которые удерживаются электростатическими или ионно-дипольными силами. Комплексы типа феррициани-да рассматривались при этом как ковалентные. [19]
Примененная к комплексам с октаэдрической конфигурацией гипотеза Таубе основывалась на популярном в то время, но неверном предположении, что dzsp3 - или внут-риорбитальные d - комплексы являются ковалентными, тогда как sp3d2 - или внешнеорбитальные d - комплексы являются ионными. У комплексов первого типа внутренняя d - орбиталь в конфигурациях d, dl и d2 остается незаполненной, что обеспечивает легкий путь для протекания реакции по ассоциативному механизму, который приводит к образованию лабильных комплексов. Поэтому можно предполагать, что реакции элементов, расположенных в этой части периодической таблицы, протекают по ассоциативному механизму. Во внешнеорбитальных комплексах, ошибочно рассматриваемых как ионные, реакции, как считали, должны протекать по диссоциативному механизму. Причем чем больше эффективный заряд на центральном атоме, тем менее лабилен комплекс. [20]
Одни комплексы легко распадаются на составные части, другие, наоборот, устойчивы. К комплексам первого типа относятся, например, некоторые галогено-комплексы ( см. ниже) и многие аквокомплексы ( какими являются, например, упомянутые на стр. В комплексах такого типа лиганды связаны с центральным ионом за счет электростатических сил притяжения ( электровалентные связи) или ион-дипольных сил ( стр. В комплексах другого типа связь между центральным атомом и лигандами не только более прочна, но и направлена в пространстве так же, как ковалентные связи в органических соединениях. Комплексы первого типа обычно называют ионными комплексами, а другие - ковалентными комплексами. [21]
Орешко, обладают различной прочностью. При низких температурах, порядка 50 - 85 С, образуются нестабильные комплексы, которые разлагаются при дальнейшем повышении температуры. Процесс хемосорбции кислорода увеличивает вес угля, а разложение нестабильных комплексов опять уменьшает вес. Температура, соответствующая максимальному приращению веса, зависит от природы угля и характеризует его склонность к самовозгоранию. При температуре выше 150 С вес угля снова увеличивается в результате образования второго типа комплексов неизвестного строения, которые обладают большей стабильностью по сравнению с комплексами первого типа и выдерживают температуру до 250 - 300 С, после чего наступает процесс горения угля с резким падением его веса. [22]
Различают ионные и ковалентные комплексы. К комплексам первого типа относятся некоторые галогено-комплексы и многие аквокомплексы. В комплексах такого типа лиганды связаны с центральным ионом диполь-ными силами. В комплексах второго типа связь между центральным атомом и лигандами более прочна и направлена в пространстве так же, как ковалентные связи в органических соединениях. Комплексы первого типа обычно называют ионными комплексами, а второго - ковалентными. Прочность комплексного иона определяется электростатическими и ковалентными силами, которые в зависимости от свойств комплексного иона могут играть преобладающую роль. Стабильность комплекса ионного типа определяется зарядом и радиусом центрального иона. Стабильность же комплекса ковалентного типа характеризуется ионизационным потенциалом центрального иона. [23]
Одни комплексы легко распадаются на составные части, другие, наоборот, устойчивы. К комплексам первого типа относятся, например, некоторые галогено-комплексы ( см. ниже) и многие аквокомплексы ( какими являются, например, упомянутые на стр. В комплексах такого типа лиганды связаны с центральным ионом за счет электростатических сил притяжения ( электровалентные связи) или ион-дипольных сил ( стр. В комплексах другого типа связь между центральным атомом и лигандами не только более прочна, но и направлена в пространстве так же, как ковалентные связи в органических соединениях. Комплексы первого типа обычно называют ионными комплексами, а другие - ковалентными комплексами. [24]
Страницы: 1 2