Эфирный комплекс
Cтраница 1
Эфирный комплекс наполовину разбавляют водой, и эфир быстро испаряют продуванием воздуха. [1]
Эфирные комплексы триалкилалюминия обычно стабильны и выдерживают перегонку. [2]
Аддукты В3Н7 с фосфорными основаниями Льюиса могут быть приготовлены из эфирных комплексов триборана. [3]
Наличие тажих соединений в продуктах реакции А1 с А1С13 и этиленом доказано выделением его эфирного комплекса и образованием C2H4D2 при разложении реакционной смеси дейтероводой. Катализатор, приготовленный в атмосфере азота, оказался неактивным при полимеризации этилена вследствие окисления субгалогенидов алюминия четыреххлористым титаном. [4]
При ведении реакции в эфирной среде в токе чистого азота нами с очень хорошим выходом был получен трифенилметил в виде его эфирного комплекса. [5]
После добавления еще 400 мл концентрированной соляной кислоты раствор снова охлаждают, встряхивают с небольшим избытком эфира и сливают нижний маслянистый слой эфирного комплекса. Эфирный комплекс выливают в склянку для отсасывания, и эфир быстро удаляют про-сасыванием воздуха через смесь при нагревании склянки на водяной бане. Это продолжают до тех пор, пока на поверхности жидкости около стенок склянки не покажутся кристаллы. Затем раствор отставляют для медленной кристаллизации или выпаривают досуха. Комплекс снова растворяют в воде и снова сушат. Эту операцию повторяют до тех пор, пока не исчезнет запах соляной кислоты. [6]
Для объяснения высоких выходов совершенно аморфного полистирола при проведении реакции в среде эфира было высказано предположение, что в этом случае в катализаторе образуются участки нестабильных эфирных комплексов, обладающих высокой активностью. На этих участках возможна случайная ориентация вступающих в реакцию мономерных молекул, приводящая к образованию аморфного полимера. Равным образом можно предположить, что эфир реагирует с гетерогенным катализатором, в результате чего непрерывно образуется свежая поверхность, обладающая высокой активностью, на которой происходит быстрая неспецифическая адсорбция мономерных молекул. В конце концов в результате реакции с эфиром катализатор полностью разрушается. [7]
Реакций со стиролом заканчивается при О С за 15 мин, а реакция с циклогексеиом и 2 3-диметилбу-теном - 2 - за 15 мин при 25 С, Эфирный комплекс трихлорборана не растворим в пентане, поэтому раствор продукта в пентане легко отделить декантацией или фильтрованием от кристаллического осадка. [8]
После добавления еще 400 мл концентрированной соляной кислоты раствор снова охлаждают, встряхивают с небольшим избытком эфира и сливают нижний маслянистый слой эфирного комплекса. Эфирный комплекс выливают в склянку для отсасывания, и эфир быстро удаляют про-сасыванием воздуха через смесь при нагревании склянки на водяной бане. Это продолжают до тех пор, пока на поверхности жидкости около стенок склянки не покажутся кристаллы. Затем раствор отставляют для медленной кристаллизации или выпаривают досуха. Комплекс снова растворяют в воде и снова сушат. Эту операцию повторяют до тех пор, пока не исчезнет запах соляной кислоты. [9]
Реакция со стиролом заканчивается при О С за 15 мин, а реакция с циклогексеном и 2 3-диметилбу-теном - 2 - за 15 мин при 25 С. Эфирный комплекс трихлорборана не растворим в пентане, поэтому раствор продукта в пентане легко отделить декантацией или фильтрованием от кристаллического осадка. [10]
Механизм реакции между смоляными кислотами и фенольнон смолой не совсем ясен. Наиболее вероятно образование эфирного комплекса, поскольку уже при простом нагревании легко получается эфир фенола и абиетиновой кислоты. [11]
А диметилмагний, оставшийся в растворе после осаждения соли, вступает во все характерные реакции. Но это еще не все - возможно образование эфирных комплексов с участием второй молекулы магнийорганического соединения. Короче говоря, в растворе этих соединений существуют сложные смеси веществ, участвующих в запутанном круговороте равновесий. Сходные процессы, очевидно, происходят и в растворах литийорганических соединений. Только там металл одновалентен, и ионы брома в дело вмешиваться не должны. [12]
В обычных условиях попытки алкилировать тетрагалогениды титана с помощью литийорганических соединений или гринь-яровских реагентов приводят к восстановлению титана ( IV) до низших валентных состояний. Однако метиллитий при - 80 реагирует с суспензией эфирного комплекса TiCU в эфире, давая летучий, но нестойкий тетраметилтитан в виде желтого вещества, которое пока еще не было получено в свободном от эфира состоянии. Тетраметилтитан разлагается при комнатной температуре и гидролизуется водой. [13]
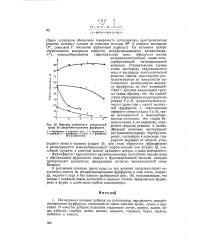 |
Влияние разбавителя реакционной среды на декарбонилирование фурфурола. [14] |
Альдегидатион реагирует далее еще с одной молекулой фурфурола с образованием эфирного иона ( стадии 4 и 5), также находящегося в хемосорбированном состоянии. Эта стадия би-молекулярна и, по-видимому, определяет скорость реакции в целом. Эфирный комплекс претерпевает внутримолекулярную перегруппировку, состоящую в перескоке гид-ридного водорбда от второго углеродного атома к первому ( стадия 5); при этом образуется фурилфуроат и регенерируется хемосорбированньщ гидроксильный ион ( стадия 6), способный служить в качестве нового активного центра, и цикл повторяется. Фурилфуроат гидролизуется адсорбированными на контакте парами воды с образованием фурилового спирта и фуранкарбоновой кислоты, которые претерпевают дальнейшие превращения согласно вышеуказанной схеме Вандора. [15]
Страницы: 1 2