Прочный комплекс
Cтраница 3
При образовании недостаточно прочных комплексов необходимо прибавление значительного избытка реактива, причем последний вводится двумя различными способами. По одному из них реактив прибавляют в некотором кратном отношении к определяемому иону. Этот способ улучшает условия определения, но не обеспечивает его точности. Конечно, всякий избыток реактива уменьшает диссоциацию комплекса, однако при несколько больших разбавлениях прямая пропорциональность между общей концентрацией определяемого иона и оптической плотностью раствора снова заметно нарушается. [31]
При исследовании очень прочных комплексов изомолярная кривая вырождается в две пересекающиеся прямые и положение абсциссы максимума на таких кривых не зависит ни от константы образования комплекса, ни от начальных концентраций реагирующих компонентов. Определение максимума на изомолярной кривой значительно затрудняется при образовании малопрочных комплексных соединений, вследствие его размытости. [32]
При образовании очень прочных комплексов с катионами кальция и магния, входящими в состав известкового налета, последний растворяется, и поверхность после смывания продуктов реакции становится совершенно чистой. [33]
При образовании достаточно прочных комплексов п-доноров с о - и - акцепторами наблюдаются, как правило, большие приросты дипольных моментов. Величина перенесенного заряда от донора к акцептору в таких комплексах сравнительно велика и, как показано в гл. I, стабилизацию таких комплексов в основном обусловливают силы переноса заряда. Вклад поляризационного взаимодействия невелик. Для комплексов типа nv и пет наблюдается определенная корреляция между дипольными моментами донорно-акцеп-торных связей и их прочностью. [34]
Таким образом, прочные комплексы ( с малой величиной Ккоипя) имеют существенные преимущества; применение таких комплексов дает возможность увеличить точность определения. Если соединение значительно диссоциирует в водных растворах, то целесообразно применять некоторые неводные растворители. [35]
Кальций переводят в прочный комплекс с сульфосалициловой кислотой. Следы Fe ( III) восстанавливают до F ( II) аскорбиновой кислотой. [36]
При рН 10 прочные комплексы с ЭДТА образуют многие металлы различной природы, поэтому для получения специфической реакции на цинк необходимо удалить или замаскировать мешающие ионы металлов. [37]
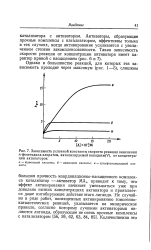 |
Зависимость условной константы скорости реакции окисления п-фенетидина хлоратом, катализируемой ванадием У, от концентрации активаторов. [38] |
Активаторы, образующие прочные комплексы с катализатором, эффективны только в тех случаях, когда активирование усиливается с увеличением степени закомплексованности. [39]
 |
Отделение железа от калия. [40] |
Металлы, образующие прочные комплексы, поглощаются анионитом, в то время как щелочные металлы беспрепятственно проходят через колонку. После промывания колонки водой щелочные металлы без труда определяются в вытекающем растворе. Если в растворе присутствует только один щелочной металл или если надо определить суммарное содержание щелочных металлов, то проще всего раствор, вытекающий из первой колонки, пропустить через другую колонку, заполненную сильноосновным анионитом в ОН-форме. Образующаяся в этой колонке едкая щелочь точно определяется титрованием стандартным раствором кислоты. Необходимо подчеркнуть, что четкое разделение достигается только при использовании силь-поосповных анионитов. [41]
Тяжелые металлы дают прочные комплексы, металлы с полностью заполненной внешней орбитой образуют мало устойчивые комплексы, например металлы первой группы: литий, калий, натрий, рубидий, цезий, а также магний, стронций, барий, алюминий, скандий, индий и др. Например, большая часть переходных металлов, отличающихся малыми размерами атомов и ионов, равно как доступностью незаполненных d - орбит, легко образуют комплексные соединения. [42]
Тяжелые металлы дают прочные комплексы, металлы с полностью заполненной внешней орбитой образуют мало устойчивые комплексы, например металлы первой группы: литий, калий, натрий, рубидий, цезий, а также магний, стронций, барий, алюминий, скандий, индий и др. Например, большая часть переходных металлов, отличающихся малыми размерами атомов и ионов, равно как доступностью незаполненных d - орбит, легко образуют комплексные соединения. [43]
Трифенилдиазениевый катион дает прочный комплекс с пиридином, вполне аналогичный аддуктам диазениевых катионов с фосфинами. Его существование обеспечивается взаимодействием НСО трифенилдиазениевого катиона с неподеленной парой атома азота в пиридине, о чем говорит отсутствие комп - лексообразования с 2 6-лутидином, где атом азота стеричес - ки экранирован. [44]
Эти элементы образуют прочные комплексы со многими неорганическими и органическими веществами, которые используются при их разделении и отделении от других ионов. Особое значение имеют комплексы с галоген-сод ержащими кислотами. [45]
Страницы: 1 2 3 4