Более прочный комплекс
Cтраница 3
Так как алюминий дает с фторидом более прочный комплекс, чем железо, и мешает титрованию, фторид предварительно отделяют от алюминия отгонкой с водяным паром. [31]
Вследствие небольших радиусов ионы плутония образуют более прочные комплексы, чем соответствующие ионы нептуния. [32]
Ряд элементов, образующих с ЭДТА более прочные комплексы - Th, Zr, Hf, Bi, Fe3, Cr3, Sc, Hg2 ( см. табл. 29) - оказывает постоянное влияние в любых условиях, однако предварительное титрование Th [551, 732, 1348, 1385] и Bi [990, 1445] при рН 1 5 - 2 0, a Sc [784, 785] при рН 2 5 позволяет внести соответствующую поправку. Рзэ еще не реагируют с ЭДТА в средах с такой кислотностью. [33]
Если же восстановленная форма связывается в более прочный комплекс, то окислительно-восстановительный потенциал системы увеличивается. IV) более прочный, чем ванадия ( V), и нормальный потенциал возрастает. [34]
Следовательно, маннит образует с галлием более прочный комплекс, чем глицерин. Известны галлаты почти всех металлов I и II групп периодической системы элементов. Галлаты щелочных металлов или аммония хорошо растворимы. Растворы галлатов по физико-химическим свойствам очень напоминают алюминатные растворы, но чрезвычайно стабильны в присутствии некоторого избытка щелочи. В противном случае они подвергаются частичному гидролизу с осаждением гидроокиси. [35]
При этом двух-зарядные анионы связываются в более прочные комплексы. [36]
Например, цитрат, который образует более прочный комплекс с празеодимом ( III), чем с церием ( III), благоприятствует отделению церия от празеодима. [37]
Установлено, что макроциклические лиганды образут гораздо более прочные комплексы, чем аналогичные лиганды нециклического строения. [38]
Перечисленные лиганды образуют с ионами М значительно более прочные комплексы, чем с ионами М что и способствует окислению. В частности, это справедливо для Со - систем. Комплекс [ Со ( Н20) б ] будет окислять воду доОа; наоборот, водные растворы солей Со легко окисляются кислородом воздуха в комплексы [ Со ( 111) Ьб ] в присутствии лигандов, таких, как NHs, CN или NOi. Значительное изменение окислительного потенциала из-за присутствия этих лигандов вызвано тем, что они создают большее кристаллическое поле, чем вода; это способствует превращению высокоспиновых - комплексов Со в низкоспиновые - комплексы Со с высокой стабилизацией кристаллическим полем. [39]
При добавлении ЭДТА ионы металла образуют с ним более прочный комплекс, и в точке эквивалентности раствор приобретает синий цвет, присущий эриохром черному Т при рН 7 - И. [40]
Отсюда видно, что бром образует с диоксаном более прочный комплекс, чем с бензолом. [41]
Так, трифенилборат образует с этиламином и пиридином более прочные комплексы, чем с ди - и триэтиламином, а 2, 4, 6-трихлор-фенилборат и2 6-диметилфенилборат вообще не образуют комплексов с пиридином. Имеется ряд интересных примеров различных сочетаний электронных и стерических факторов в донорно-акцепторных системах, содержащих арилбораты. [42]
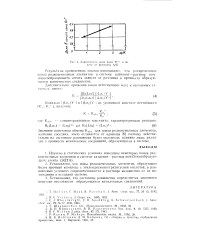 |
Зависимос П, доли иона Рг3 в ио-иите от величины ДрК. [43] |
Установлено, что ионы редкоземельных элементов, образующие более прочный комплекс с зтилендиаминтетрауксусной кислотой, в равновесных условиях сосредоточиваются в растворе независимо от их нахождения в исходной системе. [44]
Другой способ разрушения комплексных ионов основан на образовании более прочных комплексов при добавлении тех или иных реактивов. [45]
Страницы: 1 2 3 4