Поверхностный комплекс
Cтраница 1
Поверхностный комплекс при низких температурах обладает определенной прочностью, способностью длительно присутствовать на поверхности углерода, что приводит к увеличению массы нефтяного углерода, существенному изменению его поверхностной энергии и соответственно изменению физико-химических и эксплуатационных свойств. [1]
Поверхностный комплекс при низких температурах обладает определенной прочностью, способностью достаточно длительно присутствовать на поверхности адсорбционно-сольватного слоя, что может привести к увеличению массы топлива ( второй вариант), существенному изменению его поверхностной энергии и изменению физико-химических свойств топлива. [2]
Поверхностный комплекс при низких температурах обладает определенной прочностью, способностью длительно присутствовать на поверхности углерода, что приводит к увеличению массы нефтяного углерода, существенному изменению его поверхностной энергии и соответственно изменению физико-химических и эксплуатационных свойств. [3]
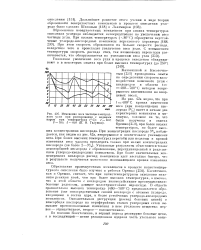 |
Изменение веса частицы электродного угля при реагировании с водяным паром при температурах ( С. 1 - 500. 2 - 550. 3 - 600 ( П. Н. Галушко. [4] |
Образование поверхностных комплексов при низких температурах окисления углерода наблюдается непосредственно по увеличению веса частицы угля. При этом скорость образования их больше скорости распада, вследствие чего и происходит увеличение веса угля. [5]
Между поверхностным комплексом, обнаруженным методом инфракрасной спектроскопии, и ацетиленовым комплексом Бика имеются два основных различия. Обычно полагают, что атомы углерода в ацетиленовом комплексе должны быть ненасыщенными, хотя сам Бик - не высказывал такую точку 70 зрения. Результаты, полученные методом инфракрасной спектроскопии, показали, что атомы углерода насыщены, даже если число атомов водорода, приходящихся на один атом углерода, мало. Вероятно, это насыщение достигается или образованием С-С связей между адсорбированными С2 - соединениями, или образованием связи между атомом углерода и двумя атомами никеля или тем и другим способом. [6]
Детальное строение поверхностных комплексов ( I -) пока не установлено, но на основе данных [18, 60] можно предположить, что комплексы ( 12) и ( 14) представляют собой солеподобные структуры типа о-толуилата и фталата. [7]
Максимальная концентрация поверхностных комплексов на поверхности нефтяного углерода соответствует его максимальной удельной поверхности и может быть зафиксирована химическими и другими методами анализа. Суммарное время, необходимое для образования и распада комплекса, величина истинной поверхности реагирования определяют в значительной мере скорость взаимодействия нефтяных углеродов с активными газами. [8]
При распаде поверхностного комплекса могут образоваться СО, СС2, Н20 и углерод ( сажа), соотношение которых зависит от размера ядра ССЕ, кинетических и диффузионных факторов и определяет суммарный тепловой эффект реакции. В избытке окислителя продукты распада комплекса - СО и С - имеют тенденцию к окислению. Это происходит в процессе сжигания топлива в избытке кислорода. При его недостатке в продуктах сгорания могут находиться СО, СО2, Н2О и С одновременно. При определенных условиях выделяющееся при реакции тепло может привести к саморазогреву топлива ( например, в присутствии катализаторов) и к его самовозгоранию. Температуру самовозгорания топлив важно знать для обеспечения правильных условий их хранения и транспортирования. [9]
Максимальная концентрация поверхностных комплексов на поверхности нефтяного углерода соответствует его максимальной удельной поверхности и может быть зафиксирована химическими и другими методами анализа. Суммарное время, необходимое для образования и распада комплекса, величина истинной поверхности реагирования определяют в значительной мере скорость взаимодействия нефтяных углеродов с активными газами. [10]
При рассмотрении поверхностного комплекса, включающего этилен CH3Ti ( Cl / 2) 4 ( C2H4), можно видеть, что основным отличием его является более низкое положение орбитали dxy из-за разрыхляющей орбитали - оле-фина. Расстояние между орбиталью а - СН3 и единственной занятой орби-талыо dxy, тем самым, уменьшается с 14900 см 1 в вакантном каталитическом центре до 11100 см 1 в комплексе. Таким образом, если расстояние от орбитали а - СН3 до следующей незаполненной или наполовину заполненной орбитали может рассматриваться как мера лабильности связи металл - - углерод, удается более количественным путем показать принцип каталитического действия иона переходного металла в реакциях полимеризации данного типа. [11]
Максимальная концентрация поверхностных комплексов на поверхности нефтяного углерода соответствует его максимальной удельной поверхности и может быть зафиксирована химическими и другими методами анализа. Суммарное время, необходимое для образования и распада комплекса, величина истинной поверхности реагирования определяют в значительной мере скорость взаимодействия нефтяных углеродов с активными газами. [12]
Технологические схемы поверхностного комплекса ледопо-родного склада ( без оборудования, размещенного в ледопородной емкости) могут быть использованы на низкотемпературных складах с металлическими и железобетонными резервуарами. [13]
Данные о поверхностных комплексах органических веществ с гексагональными фазами получены с помощью ДТА [58]; обнаружен экзотермический эффект при 400 С в пастах из СзА и 1 % глюконата кальция, глюконовой кислоты или глюкозы. В исследовании [59] показано, что молекулы органических веществ могут проникать между слоями C4AHia и образовывать гомеополярные поверхностные комплексы благодаря вандерваальсовым силам и водородным связям. [14]
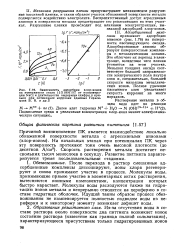 |
Зависимость адсорбции хлор-ионов на поверхности стали 12Х18Н10Т от концентрации NaCl и длительности выдержки ( цифры у кривых при потенциале коррозии данные Герасимова В. В. и др. ]. [15] |
Страницы: 1 2 3 4