Ртутный комплекс
Cтраница 3
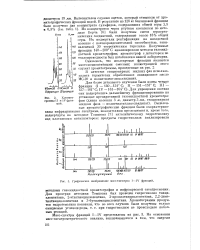 |
Графическое изображение масс-спектров I - IV фракций. [31] |
Вытеснителем служил ацетон, который отмывали от хро-матографических фракций водой. Из концентратов через ртутные комплексы по методике Берча [6] были получены смеси сераорга-нических соединений, содержавшие около 18 % общей серы. [32]
Метод основан на извлечении ртути из солянокислого раствора дитизоном ( серебро при этом связывается в AgCl) и разрушении полученного дитизоната ртути бромистым калием. В присутствии буферной смеси ртутный комплекс диссоциирует, и ион ртути титруется дитизоном. [33]
Продуктами меркурирования и последующего нитрозировани; являются ртутные комплексы о-нитрозофенолов, из которых могут быть получены соответствующие о-нитрозофенолы. Их выделение осуществляется путем разрушения ртутных комплексов кислотой с последующей экстракцией выделившихся о-нитрозофенолов. [34]
Нами была изучена реакция с водным раствором ацетата ртути меркаптанов, сульфидов и дисульфидов алифатического, нафталинового, тетрали-нового и декалинового рядов, ранее совсем не исследовавшихся в этом направлении. Одновременно был проведен анализ большинства ртутных комплексов сераорганических соединений и выяснена их структура. [35]
Реакция лучше всего протекает в случае, если. При пропускании, ацетилена в реакционную смесь образуется трудно растворимый ртутный комплекс. [36]
При действии спиртового раствора сернистого натрия ( при нагревании) на мезо-4 7-дибромдекан и рацемат - 4 7-дибромдекан были получены соответственно цис - и транс-2 5-ди-н. Для получения этих соединений в чистом виде они переводились в их ртутные комплексы, которые были многократно перекристаллизованы из этилового спирта до постоянной температуры плавления. Эти комплексы затем разлагались 15 % - ным раствором соляной кислоты, а выделившиеся тиофаны отгонялись с водяным паром, сушились над металлическим натрием и подвергались ректификации на колонке со стеклянной насадкой; погоноразделительная способность колонки была эквивалентна 27 теоретическим тарелкам. [37]
ТСХ в комбинации со спектроскопией применена Манером, Росмусом и Фабианом 8 ] для открытия, разделения и идентификации 1 2-дитиол - З - тионов, 1 2-дитиол - З - онов, их анилов, а также производных 1 2-тиазолин - 5-тионов и ксантотеновой кислоты. При исследовании сераорганических соединений нефти интересен прием, использованный авторами: ртутные комплексы сернистых соединений растворяют в ацетоне и наносят на пластинку со слоем силикагеля; стартовое пятно обрабатывают сероводородом, выделившееся сераорганическое соединение хроматографируют. [38]
В этой работе приводятся цифровые данные относительно величин скорости реакций образования и диссоциации целого ряда комплексных бромидов и иодидов, производящихся от двухвалентной ртути, кадмия и и цинка, в водных растворах. Наряду с этим было показано, что процессы изотопного обмена в более прочных ртутных комплексах протекают заметно скорее, чем в менее прочных комплексах кадмия. [39]
Сведения, приводящиеся в литературе о составе ряда ртутных производных сераорганических соединений, зачастую противоречивы. Причиной этого являются, по-видимому, различия в условиях и методах получения ртутных комплексов сераорганических соединений и отсутствие общего надежного метода их анализа. [40]
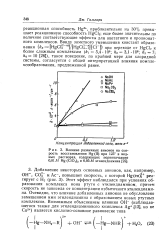 |
Влияние различных анионов на скорость восстановления Hg ( И при 123 в водных растворах, содержащих первоначально 0 01 М Hg ( С1О4 2 и 0 05 М этилендиамина. [41] |
Очевидно, что влияние добавленных анионов не обусловлено замещением ими этилендиамина с образованием новых ртутных комплексов. [42]
Сульфиты Zn и его аналогов - ZnSO3 2Н2О, CclSO3 - 2H2O и HgSO3 - малорастворимы в воде, по растворимы в растворах сульфитов щелочных металлов. Растворение обусловлено образованием комплексных солей, из которых некоторые, например Кг [ Н § ( 50зЬ ] Н2О, были получены в твердом состоянии. Ртутные комплексы этого типа устойчивы в щелочной среде, но разлагаются кислотами. В водном растворе они очень медленно распадаются по схеме: [ Hg ( SO3) 2 ] Hg - f - SO4 - j - SO. Термический распад CclSOs становится заметным примерно с 350 С. [43]
Сульфиты Zn и его аналогов - ZnS03 2Н2О, CdS03 - 2H2O и HgSO3 - малорастворимы в воде, но растворимы в растворах сульфитов щелочных металлов. Растворение обусловлено образованием комплексных солей, из которых некоторые, например К2 [ Hg ( SO3) 2 ] Н2О, были получены в твердом состоянии. Ртутные комплексы этого типа устойчивы в щелочйой среде, но разлагаются кислотами. Термический распад CdSO3 становится заметным примерно с 350 С. [44]
Эта реакция широко используется в промышленности для получения ацетальдегида из ацетилена. Эффективными катализаторами присоединения являются соли ртути. По-видимому, вначале образуется промежуточный ртутный комплекс, однако механизм реакции неясен. Первичный продукт гидратации - виниловый спирт представляет собой неустойчивый енол, который сразу изомеризуется путем перемещения активированного водорода от кислорода к углероду, образуя ацеталь-дегид. [45]
Страницы: 1 2 3 4