Координационный комплекс
Cтраница 2
Применение координационных комплексов ацетонатов ряда металлов, в частности кобальта, с пиридином и пиколином [61] значительно сокращает продолжительность отверждения эпоксидных клеев. [16]
Катализ координационными комплексами никеля важен не только с исторической точки зрения. Он имел и все еще имеет важное практическое значение для исследований превращений олефинов и диолефинов, так как типы катализируемых реакций и их условия в зависимости от окружения атома металла и степени окисления весьма разнообразны. Из различных типов превращений ненасыщенных углеводородов на никелевых комплексах мы сначала рассмотрим катализ димеризации олефинов. [17]
В координационных комплексах обнаруживаются три типа изомерии: структурная, геометрическая и оптическая. Структурные изомеры имеют одинаковую общую химическую формулу, но отличаются способами соединения составных частей. [19]
Образование таких координационных комплексов возможно потому, что алюминийалкилы и алюминийалкилхлориды являются соединениями, имеющими сродство к электрону. Алюминий на четыре валентных орбиты ( ls - орбиту и Зр-орбиты) имеет три электрона. [20]
Образование таких координационных комплексов возможно вследствие того, что алюминийалкилы и алюминийалкилхлориды являются соединениями, имеющими сродство к электрону ( алюминий на четыре валентных орбиты имеет три электрона), а соединения переходных металлов обладают электронодонорными свойствами, так как они имеют на d - орбитах, предшествующих валентным орбитам, неспаренные электроны. [21]
 |
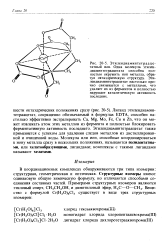
Структура иона Шесть атомов Н занимают вершины трехгранной призмы и еще три атома Н располагаются вокруг атома Re в общей с ним плоскости, параллельной основаниям призмы. [22] |
В большинстве координационных комплексов атом металла использует для образования связей меньше девяти орбиталей. [23]
Стабильность таких координационных комплексов может быть модифицирована под влиянием либо стерических факторов, либо основности самого индикатора. [24]
 |
Спектральные и магнитные свойства комплексов переходных металлов с конфигурацией d6. [25] |
Поскольку в координационных комплексах вырожденные уровни могут быть частично заполненными, из одной и той же электронной конфигурации могут возникать различные термы. [26]
Поскольку в координационном комплексе XXXVI фенильной группой гриньяровского реагента может быть оторван любой а-водород, образоваться дожен более устойчивый геометрический изомер XXXIV. Вероятно, препятствия, обусловленные мезитилыюй группой, удерживают описанные выше магниевые производные в ковалентной еполыюй форме. [27]
Окись азота образует координационные комплексы с атомами металла, которые аналогичны комплексам с окисью углерода. Однако частота валентного колебания связи азот - кислород меняется значительно сильнее в комплексах с окисью азота, чем частота связи углерод - кислород в карбонилах металлов. [28]
Красители, образующие стабильные координационные комплексы с металлами, относятся к трем основным типам: 1) азокрасителям, 2) хиноноксимам и 3) оксиантрахинонам. Общей особенностью их является наличие одной или более хелатовых групп; обычно образование хелатового кольца происходит между азо - и карбонильной группой и атомом металла, ковалентно присоединенного к кислородному атому фенольной или энольной групп. [29]
 |
Схема взаимодействия иодацетата с активным центром карбоангидразы В человека. [30] |
Страницы: 1 2 3 4