Координационный комплекс
Cтраница 3
Следовательно, структура координационного комплекса не нарушается при модифицировании гистидина. [31]
 |
Координационные комплексы. [32] |
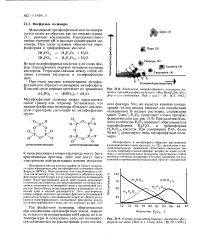
На примере ряда координационных комплексов, в которые входят Со3, NH3 и С1 -, можно дать понятие о координационной сфере и устойчивости связей между центральным атомом и входящими в сферу лигандами. [33]
Такое металлоорганическое соединение или координационный комплекс содержит электроположительный металл, в котором связь металл - углерод может рассматриваться, по крайней мере частично, как поляризованная, в результате чего углеродный атом имеет частично ионный характер и ведет себя как карб-анион. Металлоорганические соединения должны образовывать комплекс с галогенидами переходных металлов. [34]
Полифосфаты и метафосфаты образуют растворимые координационные комплексы ( см. гл. Комплексы щелочных металлов, например полиметафосфат натрия, не очень устойчивы, а щелочноземельные комплексы представляют собой вполне устойчивые соединения. [36]
 |
Хелатный комплекс кальция с этиленди-аминтетрауксусной кислотой ( EDTA. [37] |
Ионы некоторых металлов образуют индивидуально окрашенные координационные комплексы с тетрадентатными лигандами, например диметилглиоксимом. [38]
Общий механизм каталитического действия координационных комплексов сводится, как указывалось, к облегчению электронных переходов в общей системе электронов и ядер внутри комплекса, по сравнению с переходами между отдельными молекулами. В этом плане следует считать, что стадия образования координационных комплексов может ускорять как реакции окисления - восстановления, так и реакции перераспределения валентных связей ( интра - и иртер-молекулярные), поскольку между различными молекулами входящими в координационную сферу комплекса в качестве лигандов, взаимодействие облегчается. [39]
Экспериментально не обнаружено образование координационного комплекса триметилцианосилана с ВВг3, хотя характер их взаимодействия аналогичен реакции с другими тригалогенидами бора. [40]
Равновесие между двумя типами координационных комплексов зависит от состава стекла. Замена ионов кислорода на одновалентные анионы тех же размеров ведет к увеличению координационного числа катиона. Благодаря значительным силам отталкивания, действующим между такими ионами, как, например, О -, ион Si не может быть окружен больше чем четырьмя ионами кислорода. Однако во фторо-силикатах, например в Na2SiF6, ион Si, имеет координационное число шесть. [41]
Общий механизм каталитического действия координационных комплексов сводится к облегчению электронных переходов в общей системе электронов и ядер внутри комплекса, по сравнению с переходами между отдельными молекулами. С этих позиций следует считать, что стадия образования координационных комплексов может ускорять как реакции окисления-восстановления, так и реакции перераспределения валентных связей ( интра - и интермолекулярные), поскольку между различными молекулами, входящими в координационную сферу комплекса в качестве лигандов, взаимодействие облегчается. [42]
Общий механизм каталитического действия координационных комплексов сводится к облегчению электронных переходов в общей системе электронов и ядер внутри комплекса по сравнению с переходами между отдельными молекулами. В случае гетерогенного катализа через координационные комплексы можно рассматривать активный центр как металл ( его ион) с незаполненной сферой лигандов и применять к нему уже известные общие и частные принципы связи между строением комплексооб-разующего иона или ненасыщенного комплекса с его каталитической активностью. Существенную роль в определении активности катализатора в координационном катализе играют стабильность первоначально образующегося комплекса в реакциях, протекающих по механизму замещения лигандов. В этом случае, как следует из общей теории катализа и принципа энергетического соответствия Баландина, должна наблюдаться экстремальная зависимость между активностью катализатора и стабильностью комплекса. [43]
Применение аналогичного подхода к координационным комплексам требует, однако, некоторого видоизменения. Дело в том, что многие одноатомные катионы обладают электронным строением атомов благородных газов, поскольку они утрачивают свои валентные электроны в процессе ионизации ( см. гл. Таким образом, валентная оболочка изолированного катиона оказывается совершенно незаполненной. [44]
Комплекс катализатор-сокатализатор-н-мономер; инициирование координационными комплексами в средах с низкой диэлектрической проницаемостью, где акты ионизации происходят только при участии мономера. [45]
Страницы: 1 2 3 4