Активированный комплекс
Cтраница 2
Активированный комплекс возникает в качестве промежуточного состояния в ходе как прямой, так и обратной реакции. Энергетически он отличается от исходных веществ на величину энергии активации прямой реакции, а от конечных - на энергию активации обратной реакции. Эти соотношения показаны на рис. 65; видно, что разность энергий активации прямой и обратной реакции равна тепловому эффекту реакции. [16]
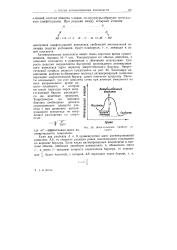 |
Энергетический профиль ре. [17] |
Активированные комплексы имеют очень короткое время существования, порядка 1СМ3 сек. Концентрации их обычно невелики, и комплекс находится в равновесии с обычными молекулами. Скорость реакции определяется быстротой прохождения активированного комплекса через вершину энергетического барьера. Благодаря накоплению энергии и сближению молекул активированный комплекс переходит энергетический барьер, давая конечные продукты. Расчеты показывают, что этот комплекс стоек при атомных смещениях во всех направлениях, кроме одного-линейного, в котором он после перехода через энергетический барьер распадается на конечные продукты. [18]
Активированные комплексы аналогичны промежуточным соединениям или адсорбированным комплексам в теориях других исследователей. Как уже отмечено выше, связи в активированных комплексах на поверхности могут быть полярными или ковалентными или представлять все переходы между этими предельными случаями. [19]
Активированный комплекс, который всегда отмечают индексом ф, является во всех отношениях обычной молекулой, за исключением того, что одна ( как правило, колебательная) степень свободы ( в направлении координаты реакции на рис. 2) у этой молекулы заменена поступательной степенью свободы. Этот вывод следует из того, что на поверхности потенциальной энергии в окрестности седло-вой точки потенциальная энергия возрастает в направлении всех координат ( что соответствует обычным колебаниям), кроме координаты реакции. Следовательно, активированный комплекс имеет четыре поступательные степени свободы и на одну колебательную степень свободы меньше, чем можно было бы ожидать. [20]
Активированный комплекс отличается от реагента главным образом отсутствием одной колебательной степени свободы. [21]
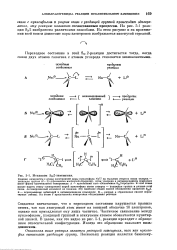 |
Механизм 8 2-замещения. [22] |
Активированный комплекс не показан. [23]
Активированный комплекс возникает в качестве промежуточного состояния в ходе как прямой, так и обратной реакции. [24]
Активированный комплекс возникает в качестве промежуточ ного состояния в ходе как прямой, так и обратной реакции. [25]
Активированный комплекс А, образующийся, по-видимому, путем удачного активирующего столкновения, представляет собой молекулу из того же числа атомов и, вероятно, не очень структурно отличается от исходной молекулы, только одна или несколько связей ослаблены. [26]
Активированный комплекс А, образующийся, по-видимому, путем удачного активирующего столкновения, представляет собой молекулу из того же числа атомов, и, вероятно, не очень структурно отличается от исходной молекулы, только одна или несколько связей ослаблены. [27]
Активированный комплекс обладает тремя поступательными ( учет одной из которых, соответствующей перемещению комплекса по координате реакции, привел к появлению множителя kT / h) и двумя вращательными степенями свободы. [28]
Активированный комплекс при мономолекулярном превращении по своим свойствам близок к исходной молекуле, однако его колебательные суммы значительно - отличаются от QKOa исходных молекул, в меньшей мере отличаются Свращ, так Как слегка изменяются межатомные расстояния. Поступательные же суммы состояний ( поскольку массы основного и активного состояний равны) будут равны и сократятся в уравнении для константы скорости. [29]
Активированный комплекс, который образуют эти ионы, содержит в качестве мостика протон. Передача этого протона - - эквивалентна передаче электрона в том же направлении. [30]
Страницы: 1 2 3 4