Адсорбированный комплекс
Cтраница 2
Это свидетельствует об участии в фарадеевском процессе лишь специфически адсорбированных комплексов. Тафелевские зависимости, полученные при постоянной поверхностной концентрации адсорбированных комплексов Г, имеют прямолинейную форму. [16]
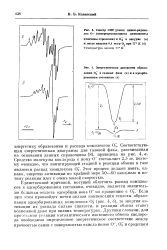 |
Спектр ЭПР [ смеси аннон-радикалов О - ( неперекрывающиеся компоненты.| Энергетическая диаграмма образования O. j в газовой фазе ( а и в адсорбированном состоянии ( б. [17] |
Если при этом произойдет почти полная компенсация теплоты образования адсорбированных комплексов Оз ( рис. 4, б), то энергия активации их распада сильно снизится, и реакция обмена станет возможной даже при низких температурах. [18]
Fc, является формальной характеристикой, поскольку в электродной реакции участвуют специфически адсорбированные комплексы. Константа & а, рассчитанная по уравнению ka j / РГ, характеризует реакционную способность адсорбированных комплексов. Видно, что константы & каж и ka сходным образом зависят от природы лиганда, находящегося в / прамс-положении по отношению к мостиковому тиоциаонат-иону. [19]
В табл. V.9 приведены кажущиеся коэффициенты переноса аг катодного процесса одноэлектронного восстановления адсорбированных комплексов Сг ( III), рассчитанные из наклона тафелевских прямых, полученных при Г const. Указанные коэффициенты переноса имеют более простой физический смысл, чем коэффициенты переноса, рассчитываемые из наклона тафелевских кривых, получаемых при постоянной объемной концентрации участвующих в реакции комплексов, когда поверхностная концентрация последних зависит от потенциала электрода. [20]
 |
Катодные и анодные поляризационные кривые, полученные с Pt-электродом при 25 С в растворе х М PtCIf, 5 1 ( Г3 М PtCl -, 1 М NaCl, 3 М H2SO4. [21] |
Полученные в работе [282] результаты свидетельствуют об участии во внутри-сферной электрохимической стадии анодного процесса адсорбированных комплексов Сг ( II), которые содержат от 1 до 3 внутрисферных мостиковых тиоцианат-ионов. [22]
В ехр ( - ДО / Г); 0 - степень заполнения поверхности электрода адсорбированными комплексами ( О Г / Г); а - аттракционная постоянная. [23]
Плотности тока обмена рассмотренных выше двухэлектронных окислительно-восстановительных систем определяются скоростью электрохимической стадии, в которой участвуют специфически адсорбированные комплексы, находящиеся в равновесии с преобладающими в растворе формами комплексов. В связи с большим различием структур исходных окисленной и восстановленной форм, участвующих в двухэлектронной реакции, перенос двух электронов между электродом и исходной частицей маловероятен. Было высказано предположение [265], что предшествующие химические реакции, в результате которых изменяется состав и структура исходных частиц ( в том числе при их адсорбции), являются необходимым условием для одновременного переноса двух электронов. [24]
Была также доказана возможность прямой гетерогенной реакции соединения молекулярных водорода и кислорода, например, на поверхности платины в адсорбированный комплекс О2 - Н2, который служит источником перекиси водорода. [25]
Высокое содержание металлов, приходящееся на единицу органического вещества, в ряде случаев можно объяснить образованием многоядерных комплексов или наличием адсорбированных комплексов, в которых имеется неэквивалентное взаимодействие между органическими лигандами и ионами металлов. [26]
Во многих случаях роль гетерогенных катализаторов в процессе окисления сводится к адсорбции органического соединения и кислорода с образованием на поверхности катализатора адсорбированного комплекса этих веществ. Такой комплекс разрыхляет связи компонентов и делает их более реакционноспособными. [27]
Таким образом, ускоряющее действие анионов, например галоид-ионов, на растворение металлов осуществляется двумя путями: во-первых, они образуют на поверхности с металлом адсорбированный комплекс, который легко теряет связь с основной массой металла и переходит в раствор; во-вторых, они устраняют пассивирующее действие кислорода, адсорбционно вытесняя его с поверхности ме-талла. Замедляющее действие атомов, например тех же галоидов, связывается с образованием прочных химических поверхностных соединении. [28]
Таким образом, ускоряющее действие анионов, например галоид-ионов, на растворение металла осуществляется двумя путями: во-первых, они образуют на поверхности с металлом адсорбированный комплекс, который легко теряет связь с основной массой металла и переходит в раствор; во-вторых, они устраняют пассивирующее действие кислорода, адсорбционно вытесняя его с поверхности металла. Замедляющее действие атомов ( тех же галоидов) связано с образованием прочных химических поверхностных соединений. [29]
Интересно отметить, что при рассмотрении схемы механизма реакции С СО2 все авторы единодушно считают, что адсорбция СО2 на углероде не имеет места или жизнь адсорбированного комплекса очень мала. [30]
Страницы: 1 2 3 4