Нейтральный комплекс
Cтраница 1
Нейтральные комплексы растворимы в органических растворителях, но нерастворимы в воде. Ацетилацетонаты имеют низкие температуры плавления ( 200 С) и испаряются без разложения. Анионные комплексы изолируют в виде солей с большими однозарядными катионами. Комплексы 8-оксихинолина применяют для аналитических целей. [1]
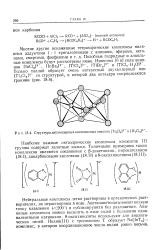 |
Структура двухъядерных комплексных анионов [ Т12С1013. [2] |
Нейтральные комплексы легко растворимы в органических растворителях, но нерастворимы в воде. Ацетилацетонаты имеют низкую точку плавления ( 200 -) и сублимируются без разложения. [3]
Нейтральные комплексы образуются при координации вокруг атома молекул, а также при одновременной координации вокруг положительного иона-комплексообразователя отрицательных ионов и молекул. [4]
Нейтральные комплексы в большинстве случаев представляют собой кристаллические солеподобные вещества. Многие из них растворимы в воде. Водные растворы большинства нейтральных комплексов не проводят электрического тока. Таким образом, нейтральные комплексы являются неэлектролитами. [5]
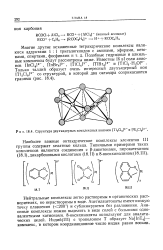 |
Структура двухъядерных комплексных анионов [ Т1гС191. [6] |
Нейтральные комплексы легко растворимы в органических растворителях, но нерастворимы в воде. Ацетилацетонаты имеют низкую точку плавления ( 200) и сублимируются без разложения. [7]
Нейтральные комплексы образуются при координации вокруг нейтрального комплексообразователя нейтральных лигандов, а также при одновременной координации вокруг положительного иона-комплексообразователя отрицательно заряженных и нейтральных лигандов. Нейтральные комплексы, следовательно, являются комплексными соединениями без внешней сферы. Чтобы отразить электронейтральность комплексов, применяют обычно русские названия комплексообразователей без изменений, а весь комплекс заключают в квадратные скобки [ Со ( МН3) зС1з1 - триамминотрихлоридкобальт. [8]
Нейтральные комплексы образуются при координации вокруг атома молекул, а также при одновременной координации вокруг по. [9]
Нейтральные комплексы образуются при координации вокруг атома молекул, а также при одновременной координации вокруг положительного иона-комплексообразователя отрицательных ионов и молекул. [10]
Нейтральные комплексы в большинстве случаев представляют собой кристаллические солеподобные вещества. Многие из них растворимы в воде. Водные растворы большинства нейтральных комплексов не проводят электрического тока. Таким образом, нейтральные комплексы являются неэлектролитами. [11]
Нейтральные комплексы не имеют внешней сферы. Заряд комплекса численно равен алгебраической сумме заряда центрального иона и зарядов лигандов. [12]
Нейтральные комплексы, внутрикомплексные соединения и ионные ассоциаты, не содержащие гидрофильных групп ( или если таких групп немного), экстрагируются из водных растворов несмешивающими органическими растворителями. В настоящее время экстракция является одним из важнейших методов разделения в химии хелатов и комплексных соединений. Преимущество метода состоит в том, что, как правило, при экстракции в органическую фазу переходят только молекулярные нейтральные комплексы. Органическая фаза представляет собой раствор только одного соединения, наряду с большим избытком реагента, а не смесь большого числа промежуточных комплексов с различными оптическими характеристиками. Кроме того, экстракция позволяет сочетать отделение определяемого элемента от мешающих ионов, маскирующих реагентов и других окрашенных компонентов раствора с одновременным обогащением. Это очень быстрый метод отделения, которое может быть выполнено при помощи простой делительной воронки. Выигрыш во времени по сравнению с методами осаждения остается даже тогда, когда небольшие коэффициенты распределения требуют или использования многократной экстракции, или более сложной операции - многократной повторной экстракции и реэкстракции. Для большинства аналитических экстракционных методов разделения необходимо перемешивание фаз в течение 0 5 - 1 мин; редко приходится сталкиваться с необходимостью более длительного перемешивания, чем 2 мин. Для того чтобы улучшить разделение фаз, собрать взвешенные капли, используют повторную экстракцию с меньшим количеством органического растворителя. Этой операции можно избежать, если не отделять экстракт полностью, а разбавлять до точного объема, особенно когда точно отмеренную часть анализируемой фазы используют для измерения. [13]
Нейтральные комплексы не имеют внешней сферы. Более сложными являются бикомплексы, состоящие из комплексных катионов и анионов. [14]
Нейтральные комплексы не имеют внешней сферы. [15]
Страницы: 1 2 3 4