Нейтральный комплекс
Cтраница 3
Концентрация нейтрального комплекса ML, ( при i y / x) если он существует, равна ПРрь постоянна и определяет тот минимум, ниже которого величина с опуститься не может. Далее по мере роста [ L ] можно достичь области, где доминируют отрицательно заряженные ( анионные) комплексы с iylx. [31]
Для катионных и нейтральных комплексов типичных окончаний нет, для анионных характерным является окончание ат или овая для названия кислот. [32]
К нейтральным комплексам относятся комплексные соединения, не имеющие внешней сферы. Поэтому нейтральные комплексы в жидком состоянии и в растворах на ионы практически не распадаются В твердом состоянии они имеют островную структуру. [33]
В нейтральных комплексах сначала перечисляются все лиганды, а в конце - называется центральный атом. [34]
Возможность экстракции нейтральных комплексов в виде неионизованных координационно сольватированных солей составляет вторую особенность рассматриваемого класса экстракционных систем. [35]
В виде координационно сольватированных нейтральных комплексов извлекаются при определенных условиях многие металлы. [36]
Помимо указанного выше нейтрального комплекса Rh ( py) 3Cl3, трихлорид родия образует с различными фосфинами и арсинами комплексы типа RhCl3L3, Rh. Родиевые соединения менее устойчивы и значительно хуже изучены, чем соединения иридия. [37]
В названиях катионных и нейтральных комплексов [ MLn ] v, [ ML ] 0 центральные атомы имеют русские наименования соответствующих элементов. Это же относится и к большинству центральных атомов в анионных комплексах [ MLn ] v -, но по традиции в этом случае для некоторых элементов используют корни их латинских наименований ( см. в гл. [38]
Таким образом, нейтральный комплекс превращается сначала в катион [ Си ( Н20) 3С1 ] зеленого цвета, а затем - в [ Си ( Н2О) 4 ] 2 голубого цвета. [39]
При этом образуется нейтральный комплекс состава 1: 1 ( один атом металла на одну молекулу красителя), так как оставшийся положительный заряд внутримолекулярно компенсируется зарядом сульфогруппы. Краситель нерастворим в воде и применяется в качестве дисперсного. [40]
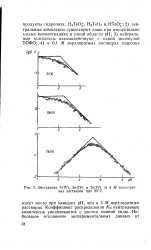 |
Экстракция S ( IV, Se ( IV и Te ( IV из 3 М перхлорат-i ных растворов при 25 С. [41] |
Коэффициент распределения Ко нейтральных комплексов увеличивается с ростом ионной силы. [42]
Почему в названиях нейтральных комплексов указание степени окисления центрального атома опускается. [43]
 |
Адсорбция Zr95 из н. HNO3. [44] |
Увеличение ван-дер-ваальсовой адсорбции нейтральных комплексов циркония в связи с фторированием поверхности объясняется ее гидрофобизацией. [45]
Страницы: 1 2 3 4