Ионизированный комплекс
Cтраница 1
Ионизированный комплекс ArHsBF способен экстрагироваться избытком жидкого фтористого водорода. Устойчивость комплексов этого типа очень сильно зависит от структуры ароматического углеводорода. Так, для м -, о - и - ксилолов она изменяется в отношении 20: 2: 1; в случае этилбензола устойчивость комплекса значительно ниже, чем для - ксилола. [1]
Образование непрочных ионизированных комплексов за счет протона и кислородного атома вещества или возникновение молекулярных соединений кислоты с исходным веществом, а также и с продуктами реакции, приводят к активированию молекул и вызывают изомеризацию, что сопровождается изменением в расположении и соотношениях электронов. [2]
Второй механизм предполагает образование ионизированного комплекса между галоидным алкилом и галогенидом алюминия ( X. [3]
Второй механизм предполагает образование ионизированного комплекса между галоидным алкилом и галогепидом алюминия ( X. [4]
Характерно, что склонность метилбензолов к образованию ионизированных комплексов в жидком фтористом водороде в отличие от их основности по отношению к хлористому и бромистому водороду резко возрастает при увеличении числа метальных групп. [5]
Цепь развивается путем последовательных присоединений изобутилена к ионизированным комплексам таким образом, что одновременно имеются растущие положительно и отрицательно заряженные цепи. Обрыв происходит в результате взаимной нейтрализации противоположно заряженных цепей. Этим объясняется, почему коэффициент обрыва уменьшается с увеличением вязкости. [6]
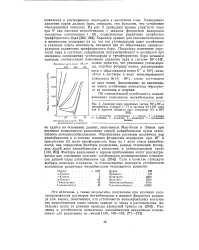 |
Давление пара различных систем HF BFs-H метилбензол ( кривые / - 7 и системы KF HF ( кривая 8, верхняя абсцисса дает отношение KF и HF. [7] |
К и HF находятся в растворе в виде ионизированного комплекса АгН BF4, также состоящего из двух ионов. Аналогичные, но значительно менее устойчивые комплексы образуются из ксилолов и толуола. [8]
Однако этот ковалентный комплекс, ионизированный в очень слабой степени, вероятно, взаимодействует с ароматическим соединением в форме ионизированного комплекса. [9]
АК в п молекулах растворителя вследствие ван-дер-ваальсо-ва взаимодействия и образования ассоциатов растворитель - ингибитор; 2-я стадия - активизация молекулы и образование ионизированного комплекса вследствие поляризации анионной и ( или) катионной части молекулы ПАВ молекулами растворителя, способных к образованию Н - связей, я-комплексов, комплексов с переносом заряда ( на протекание этой стадии большое влияние оказывает вода и другие полярные примеси); 3-я стадия - дальнейшая термическая ионизация присадки с сольватированными анионными и катионными частями, возможно образование долгоживущих свободных стабильных радикалов; 4-я стадия - электролитическая диссоциация ионизированного комплекса, происходящая в углеводородной среде только при высоких температурах к внешней поляризации электромагнитными полями высокой напряженности. [10]
АК в п молекулах растворителя вследствие ван-дер-ваальсо-ва взаимодействия и образования ассоциатов растворитель - ингибитор; 2-я стадия - активизация молекулы и образование ионизированного комплекса вследствие поляризации анионной и ( или) катионной части молекулы ПАВ молекулами растворителя, способных к образованию Н - связей, я-комплексов, комплексов с переносом заряда ( на протекание этой стадии большое влияние оказывает вода и другие полярные примеси); 3-я стадия - дальнейшая термическая ионизация присадки с сольватированными анионными и катионными частями, возможно образование долгоживущих свободных стабильных радикалов; 4-я стадия - электролитическая диссоциация ионизированного комплекса, происходящая в углеводородной среде только при высоких температурах к внешней поляризации электромагнитными полями высокой напряженности. [11]
Представляет интерес экспериментально найденная зависимость скорости фотохимической реакции от концентрации кислоты в растворе, на поверхности которого находится пленка. Она заставляет предположить, что фотолит фактически представляет собой ионизированный комплекс аммониевого или оксониевого типа. [12]
Позднее появился процесс фирмы Shell, в котором используется карбонилкобальтовый катализатор, стабилизированный фосфиновыми лигандами. При обработке октакарбонилдико-бальта триалкилфосфином выделяется окись углерода и образуется ионизированный комплекс [ Со ( СО) з ( РР з) г ] [ Со ( СО) 4 ], легко переходящий в растворимую в углеводородах форму [ Со ( СО) зРКзЬ - Последнее соединение является непосредственным предшественником активного катализатора. Ионизированный комплекс устойчив при давлениях до 0 1 МН / м2 ( 1 атм), тогда как октакарбонилдикобальт при таком низком давлении разлагается на окись углерода и металлический кобальт, который не обладает каталитической активностью. Принято считать, что активной каталитической формой является карбонилгидрид, аналогичный по своему составу соединению, получаемому из октакарбонилдикобальта, но содержащий вместо одной карбонильной группы фосфин. В качестве катализаторов гидроформилирования запатентованы также карбонилсодержащие комплексы родия; однако они пока не нашли применения в промышленности. [13]
Процесс кислотно-основного взаимодействия может остановиться на любой стадии приведенной схемы. В результате взаимодействия могут образоваться как молекулы НАВ или ионизированный комплекс НВ А и раствор неэлектролита, так и ионы НВ и А и раствор электролита. [14]
Процесс кислотно-основного взаимодействия может остановиться на любой стадии приведенной схемы. В результате взаимодействия могут образоваться как молекулы НАВ или ионизированный комплекс НВ А - и раствор неэлектролита, так и ионы НВ и А и раствор электролита. [15]
Страницы: 1 2