Роданидный комплекс
Cтраница 3
Действием раствора роданидного комплекса серебра ( при рН 5) Крафт [13] отделял небольшие количества никеля от окиси никеля, поскольку растворяется только металлический никель. [31]
Эфирный раствор роданидного комплекса ниобия имеет максимум поглощения при длине волны 385 нм. [32]
На образование роданидного комплекса ниобия значительное влияние оказывают концентрации соляной кислоты и роданида в растворе. [33]
В присутствии пиридина роданидный комплекс экстрагируется хлороформом в виде ионного ассоциата. [34]
При прибавлении фторида роданидный комплекс разрушается в результате образования бесцветного фторидного комплекса железа. Следовательно, концентрация роданида железа в последующих опытах понижается пропорционально уменьшению оптической плотности первоначального раствора. [35]
Для ускорения образования роданидного комплекса и в этом случае применяют предварительное нагревание в течение 10 - 15 мин. [36]
Максимумы оптической плотности роданидных комплексов из стандартных растворов и почвенных вытяжек близки и находятся в области 450 - 460 нм. Чувствительность метода составляет 0 1 мкг молибдена в 12 5 мл экстракта. [37]
Молярный коэффициент погашения роданидного комплекса ypana ( VI) в смеси трибутилфосфата с четыреххлористым углеродом составляет 2 9 - 103 ( удельное поглощение 0 012) при К 380 нм. [38]
Титан в виде роданидного комплекса из раствора, 6 М по хлориду ( или сульфату) и 1 М по кислоте, хорошо извлекается 0 01 М циклогексановым раствором триоктилфосфинокиси. Уран из растворов с концентрацией роданида выше 0 1 молъ / л при рН 0 5 - 2 5 экстрагируется 8 % - ным раствором ТБФ в четыреххлористом углероде. Максимум светопоглощения экстрагирующегося комплекса урана находится при 350 ммк. Окраска устойчива в течение 24 час. [39]
Железо в виде роданидного комплекса определяют фотоколориметрическим методом. При этом железо и медь уходят в фильтрат. Раствор переносят в мерную колбу емкостью 100 мл, доливают до метки водой и перемешивают. [40]
Для уменьшения диссоциации окрашенных роданидных комплексов часто применяются неводные растворители. Синий комплекс кобальта настолько диссоциирует в водном растворе, что колориметрическое определение кобальта роданидным методом в обычных условиях практически невозможно. Роданидные комплексы других металлов диссоциируют несколько меньше, однако применение и для них органических растворителей значительно повышает чувствительность и точность определений. Таким образом, этот комплекс в 90 % - ном этаноле в 2.i o - s 250 раз прочнее, чем в водном растворе. [41]
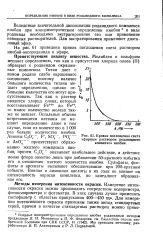 |
Кривая поглощения света. [42] |
Вследствие значительной диссоциации роданидного комплекса ниобия при колориметрическом определении ниобия в виде роданида необходимо экстрагирование его или применение неводных растворителей. Для экстрагирования применяют диэти-ловый эфир. [43]
О термодинамике образования роданидных комплексов висмута / / Журн. [44]
Для уменьшения диссоциации окрашенных роданидных комплексов часто применяются неводные растворители. Синий рода-нидный комплекс кобальта и желтый роданидный комплекс ниобия настолько диссоциируют в водных растворах, что колориметрическое их определение в обычных условиях нецелесообразно. Уменьшаются также константы всех ступеней диссоциации. Поэтому при том же общем избытке реактива все равновесия сдвигаются в сторону образования комплексов - с большим числам координированных роданид-ионов: обычно в ацетоне или при экстракции образуются тетра - и гексародани-ды. Молярные коэффициенты оветопоглощения этих комплексов значительно выше. Поэтому чувствительность определения, например, ниобия увеличивается приблизительно в 2 раза, а железа - даже более чем на один порядок. Наконец, при образовании координационно-насыщенных комплексов в неводной среде мало влияют колебания концентрации реактива. [45]
Страницы: 1 2 3 4