Аммиачный комплекс - никель
Cтраница 1
Аммиачный комплекс никеля в водном растворе устойчив. [1]
Из раствора аммиачного комплекса никеля, содержащего умеренный избыток аммиака, HzS полностью осаждает никель в виде NiS. Но если избыток NH очень велик, осаждения не происходит. Эти опытные данные можно легко объяснить. [2]
Как указывалось, аммиачный комплекс никеля обладает, хотя и незначительным, поглощением ультрафиолетовых лучей в области 360 - 380 ммк. Поэтому, чтобы избежать мешающего влияния ионов никеля, в раствор сравнения, помимо всех реактивов, вводится то же количество ионов никеля, что и в исследуемый раствор. [3]
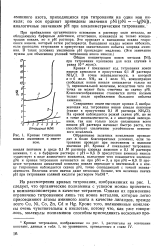 |
Кривые титрования. [4] |
В процессе титрования аммиачный комплекс никеля переходит в пентеновый и к концу титрования наблюдается скачок pNi, точно совпадающий с точкой эквивалентности. [5]
Остается выяснить, почему в системах аммиачных комплексов никеля, так же как и в аналогичных системах комплексов кобальта ( III), светопоглощение не увеличивается при введении пятой молекулы аммиака. В изученных автором системах комплексов никеля, вероятно, обе формы были почти в статистическом равновесии ( ср. Представляется поэтому справедливым положение, что замена однородно связанных молекул воды на молекулы аммиака приводит к смещению полосы поглощения в синюю область видимой части спектра и в то же время к увеличению в большинстве случаев светопоглощения. Кроме того, характерно, что степень смещения в синюю область спектра на одну молекулу аммиака [ 40 - 50 мц в системах комплексов меди ( II) и 15 - 25 м х, в системах комплексного никеля, хрома ( III) и кобальта ( III) ], по-видимому, уменьшается с увеличением координационного числа. [6]
Остается выяснить, почему в системах аммиачных комплексов никеля, так же как и в аналогичных системах комплексов кобальта ( III), светопоглощение не увеличивается при введении пятой молекулы аммиака. В изученных автором системах комплексов никеля, вероятно, обе формы были почти в статистическом равновесии ( ср. Представляется поэтому справедливым положение, что замена однородно связанных молекул воды на молекулы аммиака приводит к смещению полосы поглощения в синюю область видимой части спектра и в то же время к увеличению в большинстве случаев светопоглощения. Кроме того, характерно, что степень смещения в синюю область спектра на одну молекулу аммиака [ 40 - 50 лцл, в системах комплексов меди ( II) и 15 - 25 M L в системах комплексного никеля, хрома ( III) и кобальта ( III) ], по-видимому, уменьшается с увеличением координационного числа. [7]
В отдельной порции аммиачного раствора, возможно содержащего аммиачные комплексы никеля, кобальта и цинка, а также Мп2, обнаруживают № 2 действием ди-метилглиоксима. [8]
В отдельной порции аммиачного раствора, могущего содержать аммиачные комплексы никеля, кобальта и цинка, а также ионы Мп, откройте ион №, действием диметилглиоксима. Реакцию ведите, как описано при методе с применением перекиси водорода ( стр. [9]
Аммиачный фильтрат обрабатывают раствором цианида калия до исчезновения окраски аммиачных комплексов никеля, кобальта и меди. [10]
В последних графах табл. 2 приведены результаты аналогичных опытов с аммиачным комплексом никеля. [11]
Следует также избегать избытка аммиака, так как это способствует образованию аммиачного комплекса никеля. [12]
В патенте ЧССР [10-12] предлагается раствор химического никелирования типа ФАНИ, представляющий собой, в сущности, стабилизированный аммиачный комплекс фосфорновати-стокислого никеля. [13]
Для иллюстрации связей между Куст, Кнест, руст и ( Знест приведена таблица числовых значений этих величин для аммиачных комплексов никеля ( табл. 13.3), из которой видно, что частные константы устойчивости не очень велики. Это значит, что ли-ганд NH3 замещает в координационной сфере лиганд Н2О не очень эффективно. Видно, что эти доли сильно зависят от равновесной концентрации свободного аммиака. [14]
При определении никеля в чугунах и сталях титриметрическим методом происходит растворение никелевой соли в избытке гидроксида аммония с образованием аммиачного комплекса никеля, который затем титруют раствором цианида калия. [15]
Страницы: 1 2 3