Наиболее устойчивый комплекс
Cтраница 3
Более электроположительные металлы, например Na, Са, А1, лантаниды, Ti и Fe, относятся к классу а. Металлы класса а образуют наиболее устойчивые комплексы с лигандами, у которых донорными атомами являются элементы подгрупп N, О или F; металлы класса б предпочтительно соединяются с лигандами, в которых донорными атомами являются более тяжелые элементы подгрупп N, О или F. Предполагают, что устойчивость комплексов металлов класса б является следствием значительной доли ковалентности связей металл - лиганд и переноса электронной плотности от металла к лиганду посредством я-связи. [31]
Для металлов группы а наиболее устойчивые комплексы образуют наиболее легкие лиганды, и прочность их уменьшается по мере движения по группе сверху вниз к более тяжелым элементам. Для металлов группы б наблюдается совершенно противоположная тенденция. [32]
 |
Схема молекулярных орбит комплекса. [33] |
Как указывалось выше, наиболее устойчивые комплексы такого рода образуются катионами с заполненной d - оболоч-кой. [34]
Они являются относительно устойчивыми соединениями, разлагаясь при температурах от 0 до 160 С. Кроме возможного хемотерапевтического использования наиболее устойчивых комплексов с аминами, нитрилами, ди-кетонами и нитрофенильными соединениями никакого промышленного применения этих соединений не было предложено. [35]
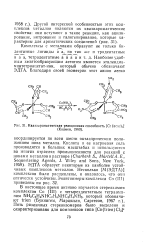 |
Квазиароматическая реакционная способность [ Сг ( асас 3 ] ( Колмен, 1963. [36] |
Кислота и ее натриевая соль производятся в больших масштабах и используются во многих отраслях промышленности для реакций с ионами металлов в растворе ( Charberk S. ЭДТА образует некоторые из наиболее устойчивых комплексов металлов. Несколько [ М ( ЭДТА) ] комплексов были расщеплены, и оказалось, что они оптически устойчивы. [37]
Ионы металлов класса ( а) образуют наиболее устойчивые комплексы с лигандами, донор ные атомы которых являются первыми элементами в каждой группе периодической таблицы. Ионы металлов класса ( б) образуют наиболее устойчивые комплексы с наиболее тяжелыми членами данной группы. [38]
Исследование реакций замещения лигандов показало, что устойчивость ацетиленовых лигандов в этих комплексах изменяется в следующем порядке: С2Н2алкилацетиленыарилаце - тиленынитроарилацетилены. Таким образом, в соответствии с предполагаемой природой связи ацетилен - металл наиболее устойчивые комплексы образуются из ацетиленов с электроно-акцепторными заместителями ( ср. [39]
Электронная конфигурация Pb ( II) [ Xe ] 4 / 145d106s2 указывает, что он легко деформируется, даже если 6х2 - электроны снижают степень образования обратной двойной связи между металлом и лигандом. Она также позволяет предположить, что РЬ ( П) должен образовывать наиболее устойчивые комплексы с сильнополяризующимися лигандами. Это подтверждается на практике. Так, РЬ ( П) лишь слабо взаимодействует с купферроном в 0 01 М азотной кислоте, а при экстракции свинца в виде его дитизоната хлороформом или четыреххлористым углеродом из водных щелочных сред могут присутствовать содержащие кислород анионы типа цитратов или тартратов. Снижение степени обратного связывания и отсутствие в комплексах РЬ ( П) стабилизации полем лигандов объясняют, почему для маскирования меди можно добавлять цианид-ионы [ образуются цианидные комплексы Cu ( I) ], не создавая помех для экстракции свинца в виде дитизоната. В общем комплексы РЬ ( П) менее устойчивы, чем комплексы Си ( II), и его дитизонат диссоциирует в разбавленных растворах минеральных кислот. [40]
При титровании ЭДТА солей металлов рН раствора уменьшается. Как показывает опыт, можно проводить определение некоторых катионов металлов, образующих наиболее устойчивые комплексы в присутствии катионов металлов, образующих комплексы с меньшей устойчивостью и разрушающихся легче в кислой среде. [41]
Смеси растворов соли данного металла и комплексообразу-ющего вещества, взятых в возрастающих молярных соотношениях первого ко второму, титруют раствором гидроокиси щелочного металла. В этом случае по перегибам на кривых титрования точно устанавливается количество молей водорода, выделившегося из комплексообразующего вещества на 1 моль металла, и отсюда находят состав наиболее устойчивого комплекса. [42]
Однако в то же время лиганды отталкиваются друг от друга, поскольку они несут одинаковые заряды либо поскольку отрицательные концы молекулярных диполей направлены к одному и тому же центру. Поэтому в любом комплексе устанавливается равновесие между силами притяжения лигандов к металлу и силами взаимного отталкивания лигандов. Наиболее устойчивый комплекс возникает при условии, что геометрическое расположение лигандов вокруг металлического центра обеспечивает максимальную величину сил притяжения между металлом и лигандами и минимальную величину сил отталкивания между лигандами. Как показано на рис. 23.22, совокупность иона металла и лигандов в комплексе имеет более низкую энергию, чем та же совокупность заряженных частиц, полностью изолированных друг от друга. [44]
Ионы металлов класса ( б) значительно - больше; они имеют более низкие положительные заряды и неспаренные валентные р-или d - электроны. Благодаря этим свойствам ионы металлов класса ( б) в большей степени поляризуемы, вследствие этого они были названы мягкими. Наиболее устойчивые комплексы эти ионы металлов образуют с донорньши атомами лигандов ( Р, S и I), имеющими низкие электроотрицательности и высокую поляризуемость. [45]
Страницы: 1 2 3 4
