Хелатной комплекс
Cтраница 1
Хелатные комплексы часто отличаются очень большей устойчивостью, в частности, в биологических условиях, а их реакция с большей частью катионов протекает очень быстро. Для комплексов ( хелатов), применяемых в качестве антидотов, как уже упоминалось, имеет значение не только устойчивость их по отношению к устойчивости тех же хелатов кальция. Эти же соотношения могут влиять и на проявление токсического эффекта ( ср. [1]
Хелатные комплексы более устойчивы, чем аналогичные комплексы с похожими по свойствам монодентантными лигандами. [2]
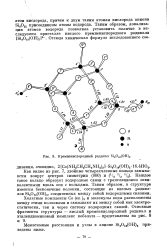 |
Кремнекислородный радикал Si8018 ( OH2. [3] |
Хелатные комплексы Со ( en) 3 и молекулы воды расположены между этими колонками и связывают их между собой как электростатически, так и через систему водородных связей. [4]
Хелатные комплексы часто отличаются очень большей устойчивостью, в частности, в биологических условиях, а их реакция с большей частью катионов протекает очень быстро. Для комплексов ( хелатов), применяемых в качестве антидотов, как уже упоминалось, имеет значение не только устойчивость их по отношению к устойчивости тех же хелатов кальция. Эти же соотношения могут влиять и на проявление токсического эффекта ( ср. [5]
Хелатные комплексы более устойчивы, чем аналогичные комплексы с похожими по свойствам монодентантными лигандами. [6]
Хелатные комплексы, по-видимому, могут быть частично активированы при адсорбции на кварце. [7]
Хелатные комплексы ( хелаты, циклические комплексы) - соединения, в которых полидентатный лиганд образует с центральным атомом цикл ( стр. [8]
Металлические хелатные комплексы были испытаны в качестве светостабилизаторов и на ударопрочном полистироле. [9]
Хелатные комплексы редкоземельных металлов и р-дикетонов представляют собой кислоты Льюиса и вызывают большие псевдоконтактные сдвиги в основаниях Льюиса, которые вводят в растворы, содержащие эти комплексы. Обратите внимание, что спин-спиновые взаимодействия все еще не затронуты. [10]
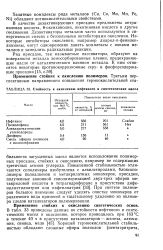 |
Стойкость к окислению нефтяного и синтетических масел. [11] |
Хелатные комплексы ряда металлов ( Си, Со, Mo, Mn, Fe, Ni) обладают антиокислительными свойствами. [12]
Образуются красно-пурпурные хелатные комплексы с железом ( II), аналогично комплексам с о-фенантролином. [13]
Образованию хелатного комплекса способствуют неполярные растворители, не способные эффективно сольватировать катион цинка, Такая трактовка механизма реакции Реформатского находится в хорошем соответствии с экспериментальными данными, согласно которым Р - и у-бромэфиры, не способные к образованию цинковых енолятов, не вступают и в реакцию Реформатского. [14]
Устойчивость хелатного комплекса является функцией не только числа членов в цикле, но и числа циклов, приходящихся на один центральный ион металла в комплексе. [15]
Страницы: 1 2 3 4