Пентакоординационный комплекс
Cтраница 2
Как мы уже видели в разд. Ci / С2 и удается наблюдать только образование пентакоординационного комплекса. В гемоглобинах и миогло-бинах, однако, энергия взаимодействия между порфирином и белком, а также расположение аминокислотных остатков таковы, что / Ci S / C2, и стабилизируется комплекс с пятью лигандами. [16]
Кислород может обратимо координироваться небелковым же-лезопорфириновым комплексом в полимерной матрице, причем грубые оценки показывают, что константа равновесия координации кислорода пентакоординационным комплексом Fe ( II) по крайней мере столь же велика, как и в случае нормальных гемоглобинов млекопитающих ( разд. В связи с этим можно сделать вывод, что после того, как белок стабилизировал пентакоординационный комплекс, никакого дальнейшего повышения прочности связи Fe - О2 не требуется, а нужна лишь тонкая регуляция в соответствии с потребностями отдельных организмов. [17]
Изучению проблемы устойчивости в случае моноолефиновых комплексов Rh ( I) и 1г ( I) посвящено мало работ. На основании имеющегося материала можно заключить, что наименее устойчивыми из них являются комплексы с С2Н4 и другими олефинами, обладающими электронодонорной двойной связью, причем особенно мало устойчивы пентакоординационные комплексы. Устойчивость пентакоординационного комплекса 1г ( С2Н4) 4С1 настолько низка, что это вещество способно существовать в атмосфере инертного газа только при температуре - 50 С. [18]
Плоские квадратные комплексы могут димеризоваться с образованием пентакоор-динационных комплексов. Константа равновесия присоединения одной молекулы основания с донорным атомом азота, например пиридина, как правило, выше, чем константа присоединения второй молекулы основания ( Ki / С2), поэтому пентакоординационный комплекс получается сравнительно легко в отличие от аналогичных комплексов Fe ( II) ( разд. [19]
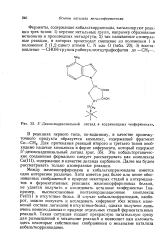 |
Дезоксиаденозильный лиганд в корриноидных кофермевтах. [20] |
Между железопорфиринами и кобальткорриноидами имеется одно интересное различие. Хотя имеется ряд более или менее обоснованных соображений о природе некоторых стадий и интермедиа - тов в ферментативных реакциях железопорфириновых белков, не удается получить и исследовать истинные коферменты [ например, высокоспиновые пентакоординационные комплексы Fe ( II) ] в отсутствие белка. В случае кобальткорриноидов, наоборот, можно получить и исследовать кофермент ( без всяких изменений состава лигандов) в отсутствие белка, однако получено лишь очень немного данных о природе отдельных стадий ферментативных реакций. Такая ситуация создает прекрасную питательную среду для размышлений о механизме реакций и позволяет нам изложить здесь некоторые собственные соображения о механизме катализа кобал ьткорри ноидами. [21]
Изучению проблемы устойчивости в случае моноолефиновых комплексов Rh ( I) и 1г ( I) посвящено мало работ. На основании имеющегося материала можно заключить, что наименее устойчивыми из них являются комплексы с С2Н4 и другими олефинами, обладающими электронодонорной двойной связью, причем особенно мало устойчивы пентакоординационные комплексы. Устойчивость пентакоординационного комплекса 1г ( С2Н4) 4С1 настолько низка, что это вещество способно существовать в атмосфере инертного газа только при температуре - 50 С. [22]
Мы убедились также в том, что локальные изменения в структуре белка ( разд. Более отдаленные изменения конформации белка, наблюдаемые на проксимальной стороне порфирина в гемоглобине, по-видимому, связаны ( или запускаются) со смещением железа по нормали к плоскости порфиринового кольца. В пентакоординационном комплексе Fe11, например, атом железа смещен примерно на 75 пм от плоскости в сторону гистидинового лиганда. Степень смещения центрального атома зависит от ионного радиуса металла ( а следовательно, от степени окисления и в еще большей мере от спинового состояния), от прочности связи с аксиальным лигандом и возмущающего влияния со стороны белка. [23]
Исследование равновесий, включающих связывание аксиальных лигандов железо ( П) порфиринами [ особенно железо ( П) протопорфи-рином ], в водном растворе затрудняется их низкой растворимостью, тенденцией к димеризации или образованию агрегатов с более высоким молекулярным весом, а также склонностью к автоокислению. В качестве основания чаще всего используют пиридин. Так называемый диакво-комплекс относится к высокоспиновым [77], однако неизвестно, содержит ли он в координационной сфере железа пять или шесть лигандов. Мы уже отметили, что пентакоордина-ционные моногистидиновые комплексы гемоглобина и миоглобина - высокоспиновые. Без сомнения, это относится и к монопиридиновому комплексу. Возьмем теперь раствор диакво-комплекса ( находящегося, вероятно, главным образом в форме димера) и будем медленно увеличивать концентрацию пиридина при полном отсутствии воздуха. Ci / G), то можно ожидать, что сначала образуется монопиридиновый, а затем дипиридиновый комплекс. Изменение спинового состояния, связанное с равновесием, характеризуемым константой Кг, очевидно, является главным фактором, который определяет знак неравенства Id Кг для железо ( П) порфиринов, хотя дополнительные осложнения возникают и вследствие изменения числа аксиальных лигандов. Поэтому не удается получить в растворе пентакоординационного комплекса железо ( П) порфирина с одной молекулой основания и изучить его реакции с кислородом. В растворах железо ( П) порфиринов в чистом сухом пиридине вообще не образуются аддукты с кислородом и не происходит окисления. [24]
Страницы: 1 2