Тиомочевинный комплекс
Cтраница 3
Определению теллура с тиомочевиной мешают Se, [ Hg2p, Pd, Os, Ph, Pt, Bi и большие количества Sb и Sn. Медь образует устойчивый тиомочевинный комплекс и не мешает определению. [31]
В каплю нейтрального или слабокислого раствора соли серебра вводится капля тиомочевинного комплекса таллия. При приготовлении тиомочевинного комплекса таллия к нитрату таллия добавляется избыток тиомочевины до перехода ярко-розового свечения в бледно-розовое. [32]
Введение тиомочевины в реакционную смесь перед облучением значительно ускоряет восстановление даже в отсутствие этанола. При облучении образуется окрашенный тиомочевинный комплекс, сильно поглощающий в области 350 - 400 нм. Оптическая плотность раствора возрастает с увеличением концентрации тиомочевины до 2 %, но при дальнейшем увеличении ее концентрации практически не изменяется. [33]
Введение тиомочевины в реакционную смесь перед облучением значительно ускоряет восстановление даже в отсутствие этанола. При облучении образуется окрашенный тиомочевинный комплекс, сильно поглощающий в области 350 - 400 нм. Оптическая плотность раствора возрастает с увеличением концентрации тиомочевины до 2 %, но при дальнейшем увеличении ее концентрации практически не изменяется. [34]
Из комплексов с тиомочевиной наиболее известен коричнево-красный ( Os ( Thio) e ] C. Значительно более разнообразны по типам тиомочевинные комплексы трехвалентных родия и иридия. Примерами их могут служить хорошо растворимый в воде желтый [ Rh ( Thio) 6 ] Cl3 и почти нерастворимый красный [ Rh ( Thio) 3Cl3 ] - Для родия и иридия довольно характерно комплексообразование также с органическими сульфидами. Зависимость растворимости от длины углеводородных радикалов проявляется здесь очень ясно. [35]
В присутствии катиона Cd2 выпадает желто-оранжевый осадок. Эта реакция позволяет открывать ионы Cd2 в присутствии ионов Си2, которые дают прочный тиомочевинный комплекс. [36]
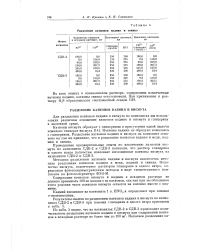 |
Разделение катионов кадмия и свинца. [37] |
Методика разделения катионов кадмия и висмута аналогична методике разделения катионов кадмия и меди, кадмия и свинца. Количество висмута, извлеченное раствором глицерина и едкого натра, определяли фотоколориметрическим методом в виде тиомочевинного комплекса на фотоколориметре ФЭК-М. [38]
Образовавшийся осадок хлорида серебра промывают водой, слегка подсушивают, смачивают раствором тиомочевины и раствором тиомочевинного комплекса таллия и рассматривают в УФ-лучах. В центре капли наблюдается люминесцирующее желтым светом пятно двойного комплекса. Медь, кадмий, олово и свинец, дающие с тиомочевиной осадки, не мешают реакции даже при 50-кратных количествах. Правда, большие количества снижают чувствительность реакции. [39]
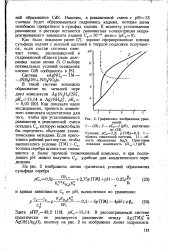 |
Графическое изображение уравнений. 7 - ( 23. 2 - рСр / ( рН, рассчитано. [40] |
Как показали наши исследования, прочность аммиачного комплекса недостаточна для того, чтобы при установившемся равновесии в реакционной смеси осталась Ср, которую можно было бы определить обычными аналитическими методами. Если приготовить рабочий раствор так, чтобы выполнялось условие [ ТМ ] Сн, то ионы серебра полностью связываются в более прочный тиомочевинный комплекс, и при подходящих рН можно получить Ср, удобные для аналитического определения. [41]
Время развития окраски - 45 мин. Окраска устойчива в течение нескольких часов. Тиомочевинный комплекс рения ( 1У) не экстрагируется органическими растворителями. Нагревание раствора способствует оптимальному развитию окраски, которое заканчивается за 5 мин. Закон Вера соблюдается в интервале концентраций 5 - 200 мкг Re / / 25 мл. Точность метода составляет 5 отн. [42]
Раствор мутится через 12 - 15 мин. Если раствор почти целиком насыщен относительно тиомочевины, то обычно осадок выпадает немедленно. Тиомочевинный комплекс меди не влияет заметно на желтую окраску от висмута. [43]
При колориметрическом определении молибдена лучшие результаты получаются при использовании роданидного метода с применением тиомочевины в качестве восстановителя. В литературе имеется указание на то, что колориметрировать молибден в растворах, содержащих висмут, можно лишь в присутствии 0 01 мг висмута в 30 мл, так как он дает окрашенный комплекс с тиомочевиной. Однако тиомочевинный комплекс висмута не экстрагируется изо-амиловым спиртом. Это дает возможность определять 0 01 мг молибдена в присутствии 2 мг висмута. В присутствии больших количеств висмута результаты определения молибдена получаются завышенными. Так, 4 мг висмута увеличивают светопогашение на 0 03, что соответствует 0 005 мг молибдена, а при содержании висмута 8 мг светопогашение увеличивается на 0 23, что соответствует 0 04 мг молибдена. [44]
При определении висмута концентрация тиомочевины должна быть больше 0 1 г-мол / л и одинакова в испытуемом и стандартном растворах. При большом относительном избытке тиомочевины висмут практически полностью находится в виде желтого комплекса. Вследствие значительной диссоциации тиомочевинного комплекса интенсивность окраски раствора сильно зависит от концентрации тиомочевины, а также от присутствия в растворе ионов, образующих с висмутом комплексы. Опыт показывает, что максимальная окраска наблюдается уже в растворе, наполовину насыщенном тиомочевиной, и не изменяется до полного насыщения раствора тиомочевиной. [45]
Страницы: 1 2 3 4