Фенантролиновый комплекс
Cтраница 2
При этом окраски комплексных соединений полностью определяются переходами с переносом заряда. Так, например, интенсивная красная окраска тиоцианат-ного комплекса окисного железа ( обычно Fe ( H2O) bCNS2) обусловлена процессом переноса заряда. То же относится к фенантролиновому комплексу закисного железа. В последнем случае, как это иногда бывает, электрон переносится от металла с низкой степенью окисления к легко восстанавливающемуся лиганду. [16]
Несмотря на то что в большинстве систем, исследуемых спект-рофотометрически, поглощает реагент или продукт реакции, это условие вовсе не обязательно, если один из компонентов может участвовать в конкурирующей реакции с образованием поглощающих соединений. Затем можно определить константу устойчивости и состав непоглощающих комплексов при условии, что имеются соответствующие данные для фенантролинового комплекса. [17]
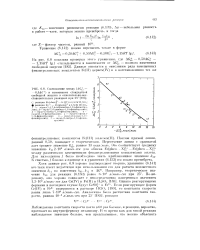 |
Соотношение между. [18] |
Наклон прямой линии, равный 0 50, совпадает с теоретическим. Пересечение линии с ординатой дает среднее значение G, равное 13 икал / моль. Это соответствует среднему значению kiz 2 - К) 3 л / моль-сек для обмена Fe ( phen - Х) - Fe ( phen - X) iJ между различными замещенными фенантролиновыми комплексами железа. Для нахождения / было необходимо знать приближенное значение kzz. К счастью, / близко к единице и в уравнении (0.153) им можно пренебречь. [19]
 |
Формальные OB потенциалы систем типа [ PtEnLCl3 ] 2 - [ PtEnLCl ] 2Cl - на фоне 1 М HCI. [20] |
Так, из табл. 12.6 видно, что замена аммиака в комплексе [ Ru ( NH3) 6 ] 3 на метиламин, бензиламин или циклогексиламин сравнительно мало сказывается на ОВ потенциалах. В то же время замена аммиака на пиридин приводит к их значительному увеличению. Потенциал растет с увеличением числа внутрисферных молекул пиридина. Дипиридильные и фенантролиновые комплексы также имеют гораздо более высокие потенциалы, чем аналогичные аммиачные. Причиной этого являются л-акцепторные свойства пиридина, дипи-ридила и фенантролина. [21]
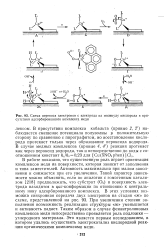 |
Схема переноса электронов с электрода на молекулу кислорода в присутствии адсорбированного комплекса меди. [22] |
В работе показано, что существенную роль играет ориентация комплексов меди на поверхности, которая зависит от заполнения и типа заместителей. Активность максимальна при малом заполнении и снижается при его увеличении. Такой характер зависимости можно объяснить, если по аналогии с гомогенным катализом [218] предположить, что субстрат ( О2) и поверхность электрода находятся в цыс-конформации по отношению к центральному иону адсорбированного комплекса. При увеличении степени заполнения возможность реализации структуры ж уменьшается и активность падает. Таким образом в случае фенантролиновых комплексов меди непосредственно проявляется роль подложки - углеродного материала. Это является первым исследованием, в котором удалось осуществить электрокатализ кислородной реак -: ции органическими комплексами меди. [23]
Страницы: 1 2