Образуемый комплекс
Cтраница 3
В случае же таких ионов, как железо ( III) и редкоземельные элементы, очевидно, больший вклад в устойчивость образуемых комплексов должен вноситься реализацией связей кислород гидр-оксила - металл. Поскольку кривая нейтрализации ОЭИДА располагается в области более низких значений рН по сравнению с кривыми ИДА и соляной кислоты ( см. рис. 36, кривые 1 - 3), можно сделать вывод, что в этой области, оттитровывается протон оксиэтильной группы. [32]
Прочность связи, зависящая от многих факторов ( заряда центрального иона, природы центрального иона и адденда, знака и величины заряда образуемого комплекса, наличия во внутренней сфере циклических группировок, включающих центральный ион, и, наконец, природы внешнесферных группировок) не может быть непосредственно приведена в соответствие с типом связи. [33]
При этом число циклов, приходящихся на один катион металла, увеличивается от семи в случае ДТПА до восьми в случае ТТГА; одновременно возрастает и устойчивость образуемых комплексов по сравнению с этилендиаминтетрацетатными. [34]
Синтезы краун-соединений с функциональными группами имеют большое значение по ряду причин: 1) функциональная группа внутри или вне краун-кольца может влиять на комплексообразование и на стабильность образуемого комплекса, 2) можно использовать реакцию по функциональной группе для получения полимерных или иммобилизованных краун-соединений. [35]
При этом число циклов, приходящихся на один катион металла, увеличивается от семи в случае ДТПА до восьми в случае ТТГА; одновременно возрастает и устойчивость образуемых комплексов по сравнению с этилендиаминтетрацетатными. [36]
Синтезы краун-соединений с функциональными группами имеют большое значение по ряду причин: 1) функциональная группа внутри или вне краун-кольца может влиять на комплексообразование и на стабильность образуемого комплекса, 2) можно использовать реакцию по функциональной группе для получения полимерных или иммобилизованных краун-соединений. [37]
Сравнение полученных нами констант устойчивости комплексов Fe3 и р.з.э. с ОПДТУ с соответствующими константами комплексов ТМТУ [15] подтверждает предположение о дополнительной координации оксигруппы ОПДТУ, так как при аналогичной структуре лигандов разница в устойчивости образуемых комплексов составляет 4 - - 5 порядков, что может быть объяснено только за счет возможной координации кислорода спиртовой группы ОПДТУ. [38]
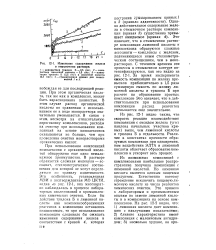 |
Изменение содержания железа в отмывочном растворе. [39] |
Из рис. 12 - 1 видно также, что скорость реакции взаимодействия композиции с оксидом железа ( угол наклона начальных участков кривых) выше, чем лимонной кислоты и трилона Б в отдельности. Различие в константах прочности образуемых комплексов при одновременном воздействии ЭДТА и лимонной кислоты облегчает образование ком-плексов и ускоряет весь процесс. [40]
Иная картина наблюдается в комплексонах на основе 2 2 -ди-фенилдиамина ( XIX-XXIII); имиподиацетатные группировки в этих соединениях сближены, что создает возможность координации металла с обеими хелатообразующими группами с замыканием максимального числа хелатных циклов, приходящихся на один катион металла. Это и приводит к увеличению прочности образуемых комплексов. К сожалению, количественная характеристика прочности комплексов отсутствует. [41]
Иная картина наблюдается в комплексонах на основе 2 2 -ди-фенилдиамина ( XIX-XXIII), иминодйацетатные группировки в этих соединениях сближены, что создает возможность координации металла с обеими хелатообразующими группами с замыканием максимального числа хелатных циклов, приходящихся на один катион металла. Это и приводит к увеличению прочности образуемых комплексов. К сожалению, количественная характеристика прочности комплексов отсутствует. [42]
Предварительные опыты, по разделению иттриевой группы редкоземельных элементов в присутствии комплексообразую-щих веществ на сульфосмолах с различным содержанием ДВЕ, показали, что при применении в качестве элюента раствора комплексообразующего вещества влияние структуры смолы сильно снижается. В этом случае главную роль безусловно играет прочность образуемых комплексов. [43]
Стабильность хелатов зависит от тех же характеристик лиганда и, кроме того, от природы атома лиганда ( донорного атома), через который осуществляется связь с центральным атомом, и степени его поляризуемости, увеличивающейся при наличии двойных связей в молекуле. Координационное число центрального атома, стереохимия и прочность образуемых комплексов определяются этими же характеристиками. [44]
Для хелатообразующих соединений характерно образование двух и более координационных связей, захватывающих центральный атом подобно клешням рака. С увеличением числа функциональных групп в молекуле комп-лексона прочность образуемых комплексов возрастает. Так, ЭДТК, имеющая шесть функциональных групп ( четыре карбоксильные группы и два атома азота), образует с металлами большое число циклов, в том числе наиболее устойчивый пятичленный, состоящий из обоих атомов азота и металла. [45]
Страницы: 1 2 3
