Дырочный комплекс
Cтраница 1
Дырочные комплексы на поверхности катализаторов представляют собой его активные центры. [1]
В образовавшемся дырочном комплексе водород играет роль ли-тийподобного иона. [2]
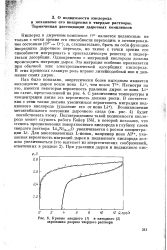 |
Кривые анодного ( 1 и катодного ( 2 заряжения разреза твердого раствора. [3] |
Кислород в дырочном комплексе 02 - является подвижным не только с точки зрения его способности переходить в активированное состояние ( 02 - - - О), и, следовательно, брать на себя функцию посредника дырочного перехода, но также с точки зрения его способности мигрировать в кристаллическую решетку и подвергаться десорбции. Одновременно с миграцией кислорода должна происходить миграция дырок. Эта миграция особенно проявляется при обычной или электрохимической адсорбциях кислорода. В этих процессах главную роль играют литийподобный ион и движение самих дырок. [4]
В действительности входящая в дырочный комплекс дырка ( Т3) представляет собой локальный избыточный положительный заряд, который компенсируется отрицательными зарядами близлежащих кислородных ионов. Дырка благодаря своему движению ( при наличии определенной энергии активации) почти одновременно может принадлежать всем ионам металла Т, составляющим первую ионную сферу вокруг подвижного иона кислорода. Таким образом, при внедрении лития и кислорода и, следовательно, при появлении Т3 одновременно вовлекаются в единую систему несколько соседних ионов металла Т, образуя так называемую внутреннюю группу твердого раствора. [5]
Q - колебательные суммы состояний дырочного комплекса и активированного комплекса; & Bl ft, F - постоянные Больц-мана, Планка, Фарадея; R - газовая постоянная; Е0 - истинная энергия активации; Т - абсолютная температура; а - доля работы для перевода из начального состояния в активированное. [6]
Эта типы хемосорбции с образованием дырочных комплексов обусловливают поверхностную электропроводность, каталитическую и электрохимическую активность окисла серебра. [7]
Таким образом, наряду с числом дырочных комплексов и подвижностью дырок большое значение для активности кислородного электрода имеет потенциал ионизации литийподобного иона. [8]
Для таких случаев и вообще для смешанных дырочных комплексов необходимо учесть также объемную дырочную электропроводность. [9]
Эти исследования убеждают, что образование поверхностных дырочных комплексов для твердых растворов ТО должно происходить по схемам (5.V) и (5.VI), следовательно, для представления механизма электрохимического процесса восстановления кислорода необходимо исходить из этих структур. [10]
Электроды, изготовленные из катализаторов с дырочными комплексами, должны быть хорошими кислородными электродами. При погружении такого электрода в раствор электролита кислород из активированного состояния легко может переходить в раствор в виде гидроксильного иона. Скорости всех этих процессов ( каталитического окисления, электролитического окисления) при отсутствии задерживающих процессов должны определяться скоростью перескока дырок. Следовательно, электропроводность этих систем ( точнее, величина плотности токообмена) должна характеризовать величину скорости указанных каталитических реакций. [11]
 |
Распределение прочностей связи при удалении дырок ( Ni3 от иона лития под действием электрического поля. [12] |
Роль же литийподобного иона заключается в первоначальном образовании дырочного комплекса, в уменьшении энергии активации дырочного перехода вблизи его ( вследствие создания некоторой асимметрии внутрикристаллического поля) и изменении энергии активации поглощения и десорбции кислорода, что опять связано с процессом образования и исчезновения дырок. [13]
Согласно приведенным схемам электрохимического восстановления кислорода на катализаторах с дырочными комплексами, скорость этого процесса и активность кислородного электрода определяются количеством ионогенных групп [ Т3 О ] ( следо-вательно, концентрацией дырочного комплекса) и энергией активации процессов дырочного перехода. Отсюда ясно, что дырочный комплекс является активным центром катализатора. Таким образом, твердые растворы, которые используются в качестве ката лизаторов кислородных электродов, должны обладать максимально возможным числом дырочных комплексов с наибольшей подвижностью дырок и кислорода. В этом отношении величина электропроводности может служить индикатором активности катализаторов, ибо, как было показано, она в такой же степени определяется концентрацией дырок и величиной энергии активации процесса и, следовательно, скоростью обмена зарядами между дырочным комплексом и двухвалентными ионами мет алла. [14]
Как и в случае окисных катализаторов, каталитическая активность угля объясняется переходом дырочного комплекса в активированное состояние при перескоке дырок. [15]
Страницы: 1 2