Диаграмма - латимер
Cтраница 2
Такие диаграммы изменения степени окисления кислотообразующего элемента и стандартных электродных потенциалов называют диаграммами Латимера. [16]
Если нужно определить значение ф окислительно-восстановительной пары по известным значениям ф других пар, используют диаграмму Латимера. [17]
Используя значение стандартных потенциалов восстановления 02 до надпероксид -, пероксид - и гидроксид-ионов, постройте диаграмму Латимера. [18]
Рассмотрим окислительно-восстановительную устойчивость переходных элементов различных степеней окисления в водном растворе, используя значения стандартных потенциалов полуреакций восстановления в форме диаграммы Латимера ( см. разд. [19]
Химия водных растворов марганца представляет особый интерес в связи с многообразием его степеней окисления. Полезным ориентиром в таком случае может служить диаграмма Латимера ( мы познакомились с такими диаграммами в разд. [20]
Диаграммы Латимера обобщают данные об окислительно-восстановительных свойствах соединений элементов. Поскольку значения потенциалов зависят от кислотности растворов, диаграммы Латимера составляют отдельно для сильно кислых ( рН 0) и сильно щелочных ( рН 14) растворов. Записывают в порядке уменьшения степеней окисления формулы тех соединений, в виде которых элемент существует в водном растворе. Для каждого из переходов указывают значения стандартных окислительно-восстановительных потенциалов. [21]
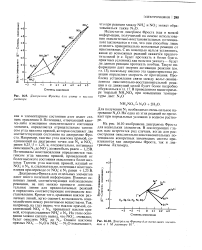 |
Диаграмма Фроста для азота в кислом растворе.| Диаграмма Фроста для нескольких элементов в 1 М растворе Н. [22] |
На рис. 16.10 изображена диаграмма Фроста для нескольких элементов. В последующих главах нам встретится ряд случаев, когда для рассмотрения окислительно-восстановительных потенциалов конкретных химических систем привлекаются как диаграммы Фроста, так и диаграммы Латимера. [23]
Концентрация катионов водорода входит в уравнение Нернста, когда ионы Н участвуют в полуреакцпях окисления и восстановления. Рассмотрим перманганат-ион как окислитель в кислотной среде. Из диаграммы Латимера, приведенной выше, видно, что стандартный потенциал восстановления иона МпО4 - до иона Мп2 равен 1 51 В. [24]
Диаграммы Латимера, суммирующие химию данного элемента в растворе, позволяют предсказать возможность дисмута-ции некоторых форм существования этого элемента. Таким формам отвечает немонотонное ( слева направо по диаграмме) уменьшение восстановительного потенциала. Подробное обсуждение диаграмм Латимера для переходных элементов приведено в разд. [25]
На мой взгляд, учебник по традиционному курсу Введение в неорганическую химию не может быть энциклопедией. Многие проблемы, рассмотренные в книге, весьма актуальны и еще дискуссионны. При изложении материала больше внимания уделено тому, чтобы осветить разные аспекты неорганической химии, а не исчерпывающе рассмотреть предмет. Чтобы дать студентам верное представление о свойствах неорганических веществ и реакциях между ними, я базировался на принципах химической связи и строения молекул, помимо этого в книге содержится достаточное количество чисто описательной химии. В третьем издании усилено внимание к окислительно-восстановительным свойствам соединений с использованием диаграмм Латимера, весьма полезных в этом случае, хотя ими и пренебрегают в последнее время. [26]
Страницы: 1 2