Неводный компонент
Cтраница 3
Для характеристики критических явлений жидкость-газ в системах, состоящих из какого-либо компонента и воды, недостаточно знания поведения ветви критической кривой, начинающейся в критической точке чистой воды. В некоторых случаях в таких - системах есть еще ветвь критической кривой, начинающаяся в критической точке неводного компонента. Такая ветвь может существовать только тогда, когда критическая температура неводного компонента выше температуры замерзания воды. Оканчивается эта ветвь в конечной критической точке ( см. гл. I), в которой критическое состояние между неводной жидкой и газовой фазами одновременно является трехфазным состоянием, т.е. критическая фаза находится в равновесии с некритической водной фазой. Если критическая температура неводного компонента невысокая, то параметры конечной критической точки мало отличаются от параметров критической точки чистого неводного компонента. Это объясняется тем, что при низких температурах давление пара воды невелико и при давлениях, близких к критическому давлению неводного компонента, содержание воды в газовой фазе, равновесной с жидкой водой, мало. При небольшом содержании воды в конечной критической точке параметры последней близки к параметрам критической точки чистого неводнопо вещества. [31]
Частичная или полная замена воды на органический растворитель для увеличения связывания реагентов в комплекс является одним из распространенных приемов спектрофотометрического анализа. Изучение комплексообразования в водно-органических растворителях показало, что в большинстве случаев наблюдается рост устойчивости комплексных соединений при увеличении концентрации неводного компонента. Для выяснения причин сложного влияния добавок органических растворителей к водным растворам на устойчивость комплексов необходимо расширение экспериментального материала. [32]
При исследовании тройных водных систем даже и при частичной кристаллизации пробы применялся иногда тип автоклава, изображенный на рис. 20, а. В этом случае отобранная проба извлекалась водой и в полученном растворе путем анализа устанавливалось отношение количеств неводных компонентов, содержание же воды в отобранных пробах рассчитывалось по соотношению количеств загруженных в автоклав воды и того неводного компонента ( соли или едкой щелочи), который, как должно быть заведомо известно, в твердую фазу не переходит ни в виде индивидуальных кристаллов, ни в виде химического соединения или твердого раствора с другим компонентом. При этом делалась поправка на количество воды, перешедшее внутри автоклава в паровую фазу. [33]
Фазовое равновесие между газом и жидкой водой существует в ограниченной области температур и давлений. Фазовое равновесие с участием жидкой воды невозможно при таких условиях, когда жидкая вода полностью превращается в лед или переходит в пар. В системах, содержащих воду и неводные компоненты, равновесие газ-жидкая вода может оказаться нереализуемым при данных условиях не только из-за невозможности существования жидкой воды, но и из-за невозможности существования газовой фазы, например, при ее сжижении или затвердевании. [34]
Большой интерес представляют исследования сжимаемости как функции температуры, так как именно в них можно наблюдать специфические свойства водных растворов. Поскольку сжимаемость чистой воды зависит от температуры немонотонно, то и водные растворы при небольших концентрациях растворенного нвэлектро1 лита демонстрируют зависимость s ( T) и т ( Т) с минимумом. Напротив, растворы с большим содержанием неводного компонента ведут себя подобно органическим веществам - сжимаемость возрастает с температурой. [35]
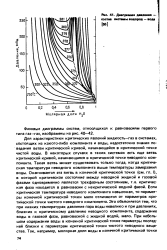 |
Диаграмма давления - состав системы водород - вода. [36] |
Для характеристики критических явлений жидкость-газ в системах, состоящих из какого-либо компонента и воды, недостаточно знания поведения ветви критической кривой, начинающейся в критической точке чистой воды. В некоторых случаях в таких - системах есть еще ветвь критической кривой, начинающаяся в критической точке неводного компонента. Такая ветвь может существовать только тогда, когда критическая температура неводного компонента выше температуры замерзания воды. Оканчивается эта ветвь в конечной критической точке ( см. гл. I), в которой критическое состояние между неводной жидкой и газовой фазами одновременно является трехфазным состоянием, т.е. критическая фаза находится в равновесии с некритической водной фазой. Если критическая температура неводного компонента невысокая, то параметры конечной критической точки мало отличаются от параметров критической точки чистого неводного компонента. Это объясняется тем, что при низких температурах давление пара воды невелико и при давлениях, близких к критическому давлению неводного компонента, содержание воды в газовой фазе, равновесной с жидкой водой, мало. При небольшом содержании воды в конечной критической точке параметры последней близки к параметрам критической точки чистого неводнопо вещества. [37]
Если нет специальных обозначений, то растворителем является вода. При использовании смесей растворителей их состав обычно выражается в весовых процентах, обозначаемых X и Y. Если одним из компонентов смеси является вода, тогда через X обозначают неводный компонент. [38]
Функции кислотности в этом случае измеряются при фиксированной концентрации кислоты и варьировании состава растворителя. За стандартное состояние обычно принимают воду, и HQ приближается к своему обычному значению в водных растворах кислот по мере того, как мольная доля Xs второго растворителя ( S) уменьшается. Для большинства растворителей электростатический вклад во взаимодействие между частицами растворенного вещества увеличивается по мере понижения диэлектрической проницаемости параллельно с ростом мольной доли Xs неводного компонента. [39]
Типичными представителями неводных компонентов, образующих системы рассматриваемого типа, являются углеводородные жидкости. В соответствии с рис. 10 в системах наблюдаются равновесия неводная жидкость-газовая фаза, водная жидкость-газовая фаза, трехфазные равновесия жидкость-жидкость-газ и равновесия жидкость-жидкость. Критическая кривая имеет две ветви: одна начинается в критической точке воды и, проходя через минимум температуры на диаграмме давление-температура, направляется к высоким давлениям и температурам; другая ветвь начинается в критической точке чистого неводного компонента и оканчивается в конечной критической точке, в которой эта ветвь критической кривой встречается с трехфазной кривой. [40]
Неводные компоненты, входящие в системы этого типа, при обычных температурах и атмосферном давлении являются жидкостями. Естественно, что при давлениях ниже давления пара или при высоких температурах они находятся в газовом состоянии. Из-за большого размера молекул эти компоненты не образуют кристаллогидратов как первого, так и второго типов. При низких температурах - в ряде случаев в этих системах неводные компоненты затвердевают. [41]
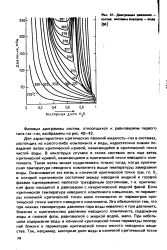 |
Диаграмма давления - состав системы водород - вода. [42] |
Для характеристики критических явлений жидкость-газ в системах, состоящих из какого-либо компонента и воды, недостаточно знания поведения ветви критической кривой, начинающейся в критической точке чистой воды. В некоторых случаях в таких - системах есть еще ветвь критической кривой, начинающаяся в критической точке неводного компонента. Такая ветвь может существовать только тогда, когда критическая температура неводного компонента выше температуры замерзания воды. Оканчивается эта ветвь в конечной критической точке ( см. гл. I), в которой критическое состояние между неводной жидкой и газовой фазами одновременно является трехфазным состоянием, т.е. критическая фаза находится в равновесии с некритической водной фазой. Если критическая температура неводного компонента невысокая, то параметры конечной критической точки мало отличаются от параметров критической точки чистого неводного компонента. Это объясняется тем, что при низких температурах давление пара воды невелико и при давлениях, близких к критическому давлению неводного компонента, содержание воды в газовой фазе, равновесной с жидкой водой, мало. При небольшом содержании воды в конечной критической точке параметры последней близки к параметрам критической точки чистого неводнопо вещества. [43]
Определение кристаллизационной воды в нерастворимых ферроцианидах металлов затрудняется тем, что эти соединения нестойки при повышенных температурах, и обычный метод потери в весе при различных температурах в данном случае зачастую оказывается неприменимым. Опыт определения гидратной воды в осадке, образуемом нитратом лантана с K4 [ Fe ( CN) e ], показал, что вода выделяется постепенно, в количестве, тем большем, чем выше температура. При этом, задолго до полной отдачи воды, соль начинает разлагаться сама, окрашиваясь в синий цвет различной интенсивности. Поэтому был разработан следующий прием. Так как состав соли по отношению к неводным компонентам во всех случаях был точно установлен, количество безводной соли в навеске могло быть точно определено, а разница в весе указывала содержание воды. [44]
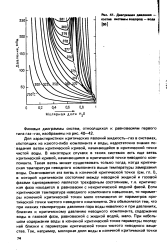 |
Диаграмма давления - состав системы водород - вода. [45] |
Страницы: 1 2 3 4