Конант
Cтраница 3
Он занимался изучением скорости восстановления цистина и некоторых других тиокислот хлоридами ванадия и хрома по методу Конанта. Ему удалось показать, что под действием хлористого хрома восстановление протекает быстрее, чем под действием хлористого ванадия, как и следовало ожидать ввиду более высокой восстановительной способности первого. [31]
В связи с этим следует указать, что начало возрастающей части необратимой полярографической волны совпадает приблизительно [184] с кажущимся потенциалом восстановления ( ARP, apparent reduction potential), которым Конант [51] характеризовал необратимые реакции с обратимыми ступенями, и который выражает окислительно-восстановительный потенциал необратимой системы посредством скорости реакции этой системы с какой-либо обратимой системой. [32]
Гидросульфит натрия применяется для восстановления ненасыщенных кетонов. Конант и Лутц [4] получили действием гидросульфита натрия в горячем спирте из симметричного дибен-зоилэтилена и его производных соответствующие дибензоил-этаны; каталитическое восстановление этих веществ, по их же данным, легко приводит к побочным продуктам. [33]
Бриджмен и Конант [5] наблюдали интересное явление: масляный и изомасляный альдегиды под давлением в 12 кбар и комнатной температуре образовывали твердые аморфные полимеры, которые при атмосферном давлении постепенно деполимеризова-лись до исходных альдегидов. Конант и Петерсон [73] позднее исследовали полимеризацию масляного альдегида подробнее. Оказалось, что на скорость этой реакции существенное влияние оказывает кислород. [34]
Бриджмен и Конант [315] наблюдали интересное явление: масляный и изомасляный альдегиды под давлением в 12 000 атм и комнатной температуре образовывали твердые аморфные полимеры, которые при атмосферном давлении постепенно деполи-меризовались до исходных альдегидов. Конант и Петерсон [350] позднее исследовали полимеризацию масляного альдегида подробнее. Оказалось, что на скорость этой реакции существенное влияние оказывает кислород. [35]
В основном электроды в водной и в неводной средах ведут себя одинаково. Конант и Чоу [143] считают, что окислительно-восстановительные потенциалы некоторых хиноидпых соединений изменяются в уксусной кислоте в зависимости от кислотности раствора. [36]
Так, Конант, Кирнер и Хасси отметили, что пространственное рассмотрение играет более важную роль для реакции присоединения, чем при реакции, включающей двойное разложение неорганических солей [ 269, стр. [37]
Так, Конант и Петерсон [22] еще в 1932 г. высказали предположение, что значительный рост скорости полимеризации ряда мономеров, вызываемый повышением давления, обусловлен, в частности, лучшей, более благоприятной для реакции взаимной ориентацией молекул мономера под давлением. [38]
Ослабляв и дифференцируя силу кислот, уксусная кислота усиливает и нивелирует силу оснований. Подробные исследования Конанта и Хелла, Хелла и других авторов показали, что вещества, обладающие очень слабо выраженными основными свойствами, проявляют в уксусной кислоте заметные основные свойства. [39]
Ослабляя и дифференцируя силу кислот, уксусная кислота усиливает и нивелирует силу оснований. Подробные исследования Конанта и Хелла, Хелла и других авторов показали, что вещества, обладающие очень слабо выраженными основными свойствами, проявляют в уксусной кислоте заметные основные свойства. [40]
Большое значение имеет обобщение, относящееся к области органических соединений, способных подвергаться металлированию. В отличие от Конанта, исследовавшего относительную кислотность соединений, К. А. Кочешков и Т. В. Талалаева иодмечают значительно более широкие связи среди различных критериев оценки относительной кислотности веществ. Наряду с экспериментальными данными, они привлекают факторы химического строения и поэтому выявляют более точные закономерности. Вместо ряда Конанта эти закономерности они выражают таблицей, которая содержит металлирующиеся вещества, начиная от инертных углеводородов и кончая соединениями с весьма подвижным водородным атомом. [41]
Кислотность ряда полиарилметанов была определена при изучении равновесий металлоорганических соединений в неполярных растворителях. Первые исследования такого рода были проведены Конантом и Виландом [ 181 в 1932 г. В эфирном растворе были получены равновесные смеси двух углеводородов и их натриевых или калиевых солей; концентрацию карбанионов в смеси определяли двумя путями. Во-первых, определяли окраску каждого аниона отдельно и по окраске равновесной смеси устанавливали положение равновесия. Во-вторых, в равновесную смесь пропускали двуокись углерода и определяли, какая часть каждого углеводорода превращается в карбоновую кислоту. Первый колориметрический метод является только качественным; второй метод может быть количественным, однако он основан на предположении, что реакция натриевых и калиевых солей углеводородов с двуокисью углерода достаточно быстрая и не смещает положения равновесия. [42]
Такой подход был сделан впервые в 1932 г. Конантом и Уэландом [19], которые установили первую шкалу относительной кислотности С - Н - кислот. В настоящее время рассмотрение реакции металлирования как кислотно-основного взаимодействия находит все более широкое распространение. [43]
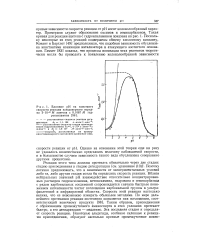 |
Влияние рН на константу скорости реакции псевдопервого порядка 5 - 10 - 4УИ ацетона с 0 0167 М гид-роксиламина [ 98 J. [44] |
Примерами служит образование оксимов и семикарбазонов. Поскольку некоторые из этих реакций подвержены общему кислотному катализу, Конант и Бартлет [49] предположили, что подобная зависимость обусловлена константами ионизации катализатора и атакующего азотистого основания. [45]
Страницы: 1 2 3 4